توضیحات
ادتا 4 سدیم یکی از ترکیبات مفید در صنایع مختلفی مانند تولید شوینده ها، تصفیه آب و غیره است. جهت ثبت سفارش و اطلاع از قیمت فروش و خرید ادتا 4 سدیم با کارشناسان ما تماس حاصل فرمایید. در ادامه با این ماده و خواص کلاته کنندگی آن بیشتر آشنا خواهید شد پس با ما همراه باشید.
خرید ادتا 4 سدیم :
موسسه مبتکران شیمی مفتخر است که توانسته سهم کوچکی در چرخه تامین کالای مورد نیاز تولیدکنندگان عزیز داشته باشد و شما را در زمینه خرید ادتای مورد نظرتان یاری نماید.
فروش ادتا :
موسسه مبتکران شیمی فعال در زمینه فروش انواع مواد شیمیایی این محصول را با بهترین کیفیت و بهترین قیمت به مشتریان ارائه می کند برای آگاهی از آخرین قیمت ادتا 4 سدیم با شماره های زیر تماس حاصل بفرمایید:
قیمت ادتا 4 سدیم :
برای آگاهی از قیمت با کارشناسان فروش ما در ارتباط باشید.
ادتا 4 سدیم چیست؟
ادتا 4 سدیم (Tetrasodium EDTA) یا اتیلن دی آمین تترا استیک اسید با فرمول شیمیایی C10H12N2Na4O8، ماده ای بی رنگ یا پودر سفید رنگ و محلول در آب است. به عنوان یک ترکیب کلاته کننده برای رفع مسمومیت فلزی، عامل ضد خوردگی و تصفیه آب کاربرد دارد. تترا سدیم ادتا را از واکنش اتیلن دی آمین، فرمالدهید و سدیم سیانید تهیه می کنند.
خواص و ویژگی ها
| ساختار | 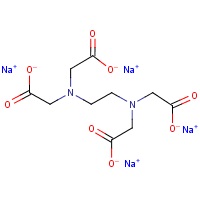 |
| فرمول شیمیایی | C10H12N2Na4O8 |
| وزن مولکولی | 380.2 g/mol |
| مشخصات ظاهری | ماده ای بی رنگ |
| حلالیت | محلول در آب |
این ماده یک ترکیب کلاته کننده است که می تواند فلزاتی مانند کروم ، آهن ، سرب ، جیوه ، مس ، آلومینیوم ، نیکل ، روی ، کلسیم ، کبالت ، منگنز و منیزیم را غیر فعال نماید. با کلاته نمودن عناصر فلزی این ترکیبات دیگر اثری بر بدن نخواهند داشت و دفع می گردند. به دلیل همین خاصیت این ترکیب یک داروی موثر برای رفع مسمومیت های فلزی و یک عامل ضدخوردگی و تصفیه ی آب به دلیل کلاته نمودن یون های کلسیم و منیزیم به حساب می آید.
تولید
این ترکیب بری اولین بار در سال 1935 توسط مونز در اثر اختلاط اتیلن دی آمین و کلرو دی استیک اسید ایجاد شد.امروزه EDTA از واکنش اتیلن دی آمین، فرمالدهید و سدیم سیانید سنتز میشود.این مسیر منجر به تولید نمک سدیم شده که در مرحله بعدی تبدیل به اسید میشود.
H2NCH2CH2NH2 + 4CH2O + 4NaCN + 4H2O → (NaO2CCH2)2NCH2CH2N(CH2CO2Na)2 + 4NH3
(NaO2CCH2)2NCH2CH2N(CH2CO2Na)2 + 4HCl → (HO2CCH2)2NCH2CH2N(CH2CO2H)2 + 4NaCl
این فرآیند سالانه برای تولید 80 هزار تن EDTA صورت می گیرد.
کاربرد ادتا 4 سدیم
محصول فوق برای انحلال رسوبات آهکی به طور گسترده ای استفاده می شود. مورد عمده مصرف این ماده در جداسازی یون های فلزی موجود در محلول های آبی است. در صنعت نساجی ضمن گرفتن یون ها، از ایجاد ناخالصی در رنگ های سنتز شده جلوگیری کرده و مانع از تغییر رنگ آنها میشود. در صنعت خمیر و کاغذ از عملکرد یون های فلزی به خصوص از (Mn(II خودداری کرده و با مهار آنها کاتالیز نامتناسب هیدروژن پر اکساید (که به عنوان سفید کننده فاقد کلر شناخته می شود) را متوقف می کند. به علل مشابه به برخی مواد غذایی افزوده می شود تا مدت نگهداری آنها را افزایش دهد.
کاهش سختی آب در لباسشویی ها و همچنین در مقیاس های بزرگتر در دیگ های بخار مربوط به اتصال یون های Ca+2, Mg+2 و سایر یون های فلزی است. که در این مورد نیز از EDTA استفاده می شود . در حضور EDTA یون های فلزی رسوب می کنند به همین دلیل در اکثر شوینده ها از این ماده استفاده می شود.
حل کردن یون های آهن توسط ادتا میتواند در pH خنثی و یا اسیدی انجام شود. این ویژگی در بخش کشاورزی خصوصا کشت های هیدروپونیک(آب پایه ) اهمیت اساسی دارد. البته با توجه به این نکته که تشکیل لیگاند وابسته به اسیدیته است EDTA در بهبود حلالیت آهن در خاک های خنثی تاثیری ندارد. به عبارت دیگر در pH نزدیک خنثی و بالاتر از آن ، آهن (III) به شکل نمک نامحلولی در می آید، که دسترسی کمتری به گونه های گیاهی حساس دارد و مطلوب نیست.

نحوه جداسازی یون های فلزی
ادتا 4 سدیم یک کلاته کننده است. ترکیبات آلی که یون های فلزی را در ساختاری دایره وار (کلات های دایره ای) هماهنگ می کنند به عنوان عوامل کلاته کننده شناخته می شوند. اکثر کلاته کننده ها دارای اکسیژن ، نیتروژن و گوگرد در مولکول های خود هستند. کلات های دارای 5 و یا 6 حلقه پایدارترین ساختارها را دارند. در واکنش کلاته کننده های معمول مانند اتیلن دی آمین ، استیل استون و اکسین چندین مولکول با یک یون فلزی مجموعه ای هماهنگ را تشکیل می دهند. ادتا که دارای اتم های هماهنگ زیادی است ، کلات بسیار پایداری را بین یک مولکول از ادتا و یون فلزی برقرار می کند.
از این ترکیبات برای تیتراسیون کلاته ، و جداسازی یون های فلزی استفاده می شود. همچنین برای پوشش یون های خاص ، پایدار کردن فلزات در حلال های آلی و کروماتوگرافی گازی یون های فلزی از کلاته کننده هایی مانند EDTA استفاده می شود.
فروش و خرید ادتا 4 سدیم با بهترین کیفیت و قیمت در مبتکران شیمی
حذف هیدروژن سولفید از جریان گاز
ماده ی فوق برای حذف هیدروژن سولفید از جریان گاز نیز مورد استفاده قرار میگیرد. در این تبدیل هیدروژن سولفید به عنصر گوگرد اکسید میشود:
H2S +2[Fe(EDTA)]− → 2[Fe(EDTA)]2- + 2H++ S
این ماده در جداسازی فلزات لانتانید توسط کروماتوگرافی تبادل یونی نیز کاربرد دارد. تبادل یونی امروزه به عنوان تنها روش ایجاد لانتانیدها با درصد خلوص بالاست.
صنایع داروسازی
EDTA در لیست سازمان بهداشت جهانی به عنوان یکی از داروهای بسیار مهم تلقی می شود.
این ترکیب برای درمان مسمومیت به سرب و جیوه مورد استفاده قرار می گیرد. همچنین برای حذف آهن اضافی از بدن برای درمان عوارض ناشی از تزریق های مکرر در بیماران مبتلا به تالاسمی کاربرد دارد.
در دندانپزشکی برای حذف باقیمانده های موجود در کانال ریشه و آماده کردن آن برای پر کردن دندان مورد استفاده قرار می گیرد. قطره های چشمی نیز حاوی این ماده هستند که نقش آن افزایش زمان ماندگاری محصول می باشد.
[(Cr(EDTA] در ارزیابی عملکرد کلیه نیز مورد استفاده قرار می گیرد به این صورت که به صورت داخل وریدی تزریق می شود و از میزان خروج آن از ادرار برای ارزیابی میزان تصفیه گلومرولی استفاده می کنند.
برخی پزشکان معتقدند EDTA به عنوان یک آنتی اکسیدان عمل می کند و از اتصال رادیکال های آزاد به دیواره سلول های خونی جلوگیری می کند.
کاربرد در شوینده های صنعتی
ادتا 4 سدیم از رسوب کردن کلسیم، منیزیم و فلزات سنگین که می توانند باعث ایجاد رسوب در محفظه ها، لوله ها، نازل ها و سایر تجهیزات شوند جلوگیری می کند.
کاغذ و نساجی
عوامل سفید کننده توسط تولیدکنندگان کاغذ برای حذف لیگنین از الیاف سلولز و بهبود روشنایی مورد استفاده قرار می گیرد. اگر هیدروژن پراکسید به عنوان عامل سفیدکننده استفاده شود، فلزات سنگین مانند منگنز پراکسید را تجزیه می کنند از این رو باید کلاته شوند. برای کلاته کردن این فلزات سنگین از ادتا چهار سدیم می توان استفاده کرد.

آبکاری فلزات
از این ماده برای تولید مدارهای چاپی استفاده می شود. عموما در آبکاری مس استفاده می شود، هنگامی که مس در طی کاهش کاتالیستی ترکیبات حاوی مس بر روی مدار رسوب داده می شود.
تصفیه آب
در فرآیندهای تصفیه از این نمک برای پاک کردن رسوبات موجود در سطوح داخلی دیگ بخار و همچنین در ترکیب با آب ورودی برای جلوگیری از تشکیل رسوبات کلسیم و منیزیم استفاده می شود.
پلیمر و لاستیک سازی
در تولید الاستومرهای بوتادین استایرن که عموما توسط پلیمریزاسیون امولسیونی انجام می شود از این کلاته کننده برای کنترل یون های Fe2+ و Fe3+ استفاده می شود.
ایمنی ادتا 4 سدیم
EDTA سمیت حاد ایجاد میکند(LD50 (rat) of 2.0 – 2.2 g/kg). این ماده دارای خاصیت تجمع زیستی است و از این نظر برای محیط زیست و موجودات آن ایجاد خطر میکند.
پرسش و پاسخ :
1- کاربرد این ماده در شامپوها چیست؟

شامپوها به کمک عوامل کف زا موسوم به سورفکتانت در فرمولاسیون خود باعث شستشوی بهتر و جداسازی آلودگی از سطح مو و پوست می شوند،در مواردی وجود یونهای فلزی همچون کلسیم و منیزیم در آب، باعث سختی آن و عدم عملکرد مناسب سورفکتانت های موجود در شامپو ها می شود،اینجاست که ادتا4سدیم با خنثی سازی این یون های فلزی عملکرد عوامل کف زا (سورفکتانت ) را بهبود بخشیده و شستشو را بهبود می بخشد.
جهت خرید و اطلاع از قیمت ادتا با شماره های واحد فروش تماس حاصل فرمایید.














نقد و بررسیها
هنوز بررسیای ثبت نشده است.