توضیحات
اسید فسفریک (Phosphoric acid) یک اسید بدون رنگ و بو است که فرمول H3PO4 را دارد و به صورت گسترده ای در صنایع تجاری و غذایی استفاده میشود. این ترکیب بسیار خورنده است و معمولا به عنوان نگهدارنده و همچنین به علت داشتن طعم تند و تیز در نوشیدنی ها استفاده می شود. یکی از مهم ترین کاربردهای این اسید در کشاورزی است که برای تامین فسفر مورد نیاز گیاهان مورد استفاده قرار میگیرد. اگرچه در دسته اسیدهای قوی قرار نمی گیرد اما تحریک کننده و خورنده پوست، چشم و سایر غشاهای مخاطی است در حالیکه نمک های آن خورندگی خیلی کمتری دارند. محصول مذکور به دو شکل مایع و جامد وجود دارد که شکل مایع دارای خلوص 85 درصد است، همچنین از نظر کاربرد می توان دو گرید صنعتی و خوراکی را برای آن نام برد. برای خرید اسید فسفریک خوراکی و اطلاع از قیمت فروش آن با ما در تماس باشید.
خرید اسید فسفریک
این اسید در گریدهای خوراکی و صنعتی با خلوص 85 درصد آماده فروش و ارسال به تمام نقاط ایران در کمترین زمان ممکن است. اطلاعات مورد نیاز برای خرید این اسید معدنی را می توانید در جدول زیر مشاهده نمایید.
خرید اسید فسفریک صنعتی
گرید صنعتی این اسید به صورت گسترده در صنایعی مانند تولید کودهای شیمیایی، تولید محصولات بهداشتی و آرایشی و … مورد استفاده قرار می گیرد. اگر به دنبال محصولی با کیفیت، به صرفه و تجربه نمودن یک خرید عالی هستید، جای درستی را انتخاب کرده اید.
خرید گرید خوراکی
این اسید به دلیل مزه خاص و خاصیت اسیدی که دارد در تولید بسیاری از نوشیدنی ها و محصولات غذایی مورد استفاده قرار می گیرد.
قیمت اسید فسفریک
| گرید خوراکی برند کمکس (85%) |
78000 تومان (گالن 35 کیلویی و مخزن 1650 کیلویی) |
اسید فسفریک چیست؟
اسید فسفریک (Phosphoric acid) با نام آیوپاک ارتوفسفریک اسید ترکیبی معدنی با فرمول شیمیایی H3PO4 است. این اسید معدنی مایعی بی رنگ، بدون بو، غیر فرار و کریستالی است. اسیدی قوی نیست اما محرک و خورنده است. از این اسید در صنایع غذایی به عنوان نگهدارنده و در کشاورزی برای افزایش رشد گیاهان استفاده می کنند.


این اسید معدنی یک اسید تری پروتیک است که به صورت مایع با چگالی بالا وجود دارد، امتزاج پذیر با آب است و از آن چگال تر است. وقتی در آب باشد هیدرولیز می شود و حرارت زیادی ایجاد می کند. این اسید یک ترکیب کیلیت دهنده است و اگر روی فلزات قرار بگیرد می تواند باعث خوردگی آن ها بشود.
پودر اسید فسفریک:
این ماده به دو صورت مایع و جامد وجود دارد که نوع مایع آن میزان خلوص 85 درصد دارد، اما نوع جامدش کاملا خالص و پودری شکل است. اسید فوق می تواند به عنوان یک جدا کننده عمل کند و به بسیاری از کاتیون های دوظرفیتی مانند Fe2+، Cu2+ و Mg2+ متصل شده و آن ها را از محیط مورد نظر جدا کند، بنابراین می توان آن را به عنوان یک نرم کننده در آب سخت در نظر گرفت. این ترکیب به علت ارزان و در دسترس بودن کاربردهای بسیار زیادی در صنعت دارد.
اسید فسفریک 85 درصد:
این اسید با خلوص 85 درصد، برای کاربردهای صنعتی و خوراکی مورد استفاده قرار می گیرد.
خواص فیزیکی و شیمیایی:
در ادامه ساختار و برخی خواص فیزیکی آن را مشاهده می کنید:
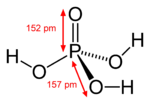
| خواص | توضیحات |
| فرمول شیمیایی | H3PO4 |
| جرم مولی | 97.994 گرم بر مول |
| چگالی (دمای 25 درجه سانتیگراد) | مایع : 1.6845 گرم بر مترمکعب
جامد: 1.834 گرم بر مترمکعب |
| نقطه ذوب | 40-42 درجه سانتیگراد |
| نقطه جوش | 212 درجه سانتیگراد |
| حلالیت | محلول در آب، اتانول و مخلوط اتر-الکل |
| pH (در محلول 1/0 نرمال) | 1.5 |
خواص اسیدی
ظرفیت این اسید نسبت به هیدروژن هایی که دارد متناسب با 3 می باشد. هرسه هیدروژن موجود در این اسید، خاصیت اسیدی دارند و به ترتیب دارای ثابت تفکیک pKa1=2.14، pKa2=7.20 و pKa3=12.37 هستند. در محلول های آب، این ماده بیشتر به ترکیبی از سه آنیون آن تفکیک می شود، به جز در pH بسیار پایین که معادلات تعادلی آن در زیر مشاهده می شود:
H3PO4 + H2O ⇌ H3O+ + H2PO4− Ka1= 7.25×10−3 [pKa1 = 2.14]
H2PO4−+ H2O ⇌ H3O+ + HPO42− Ka2= 6.31×10−8 [pKa2 = 7.20]
HPO42−+ H2O ⇌ H3O+ + PO43− Ka3= 3.98×10−13 [pKa3 = 12.37]
انواع اسید فسفریک:
از لحاظ گرید می توان آن را به دو دسته ی صنعتی و خوراکی تقسیم بندی کرد. اما از نظر روش تهیه آن را به دو دسته ی:
- اسید خام: از سنگ فسفات تهیه می شود
- اسید با خلوص بالا: از فسفر سفید به دست می آید
تقسیم بندی کرد.
فرآیند تولید فسفریک اسید
این اسید ضعیف را می توان با سه روش تجاری: فرآیند مرطوب، فرآیند حرارتی و فرآیند کوره خشک تولید کرد که در ادامه به شرح آنها خواهیم پرداخت:
فرآیند مرطوب :
رایج ترین و مطلوب ترین روش فرآیند مرطوب است که بیشتر برای تولید کودهای فسفاته استفاده می شود. در این روش سنگ های معدنی حاوی فسفات مانند کلسیم هیدروکسی آپاتیت با اسید سولفوریک طبق معادله زیر واکنش می دهد که طی این واکنش اسید تولید و رسوب سولفات کلسیم به عنوان محصول جانبی ته نشین می شود:
Ca (PO4)3OH + 5H2SO4 → 3H3PO4 + 5CaSO4 + H2O
فرآیند حرارتی :
در فرآیند حرارتی، محصول تولید شده خلوص بسیار بالایی دارد و در ساخت مواد شیمیایی با خلوص بالاتر مانند داروها، مواد شوینده، محصولات غذایی و سایر محصولات به غیر از کود استفاده می شود به این صورت که عنصر فسفر با اکسیژن ترکیب می شود و فسفروس پنتا اکسید تولید می شود. در ادامه فسفروس پنتا اکسید را هیدراته کرد و محصول اسید مورد نظر تهیه می شود. آلاینده اصلی حاصل از فرآیند حرارتی، ذرات معلق، به شکل غبار اسیدی است.
P4 + 5O2 → 2P2O5
P2O5 + 3H2O → 2H3PO4
روش کوره خشک :
به علت کاهش اثرات زیست محیطی و همچنین صرفه جویی بالا در هزینه تولید، یک روش امیدوار کننده محسوب می شود. در این روش سنگ معدن فسفات با ترکیب شدن با یک منبع کربن، سیلیکا و گرما احیا می شود. این فرایند از کنترل هوا برای کنترل میزان سوختن گازهای تولید شده از بستر کوره به منظور کنترل دمای بالای کوره استفاده می کند.
کاربرد
این اسید در دو گرید استفاده می شود که شامل گرید خوراکی و صنعتی و کشاورزی هستند. شرح موارد کاربرد را در ادامه بررسی می کنیم :
کاربرد اسید فسفریک خوراکی :
این اسید با درجه غذایی (افزودنی E338) برای اسیدی کردن غذاها و نوشیدنی ها مانند نوشیدنی های کولا (نوشابه ها) استفاده می شود. از آنجا که این ماده ارزان است استفاده زیادی از آن می شود و به هر ماده غذایی اضافه می شود طعم آن را ترش می کند. همچنین به عنوان تقویت کننده طعم، ماده شفاف کننده، ماده نگهدارنده و ماده اسیدی به غذاها افزوده می شود. نوشابه ها از جمله محصولاتی هستند که حاوی این اسید در گرید خوراکی می باشند. اسید فسفریک در نوشابه در گرید خوراکی بیشترین استفاده را دارد.
اسید فسفریک در نوشابه:
تقریبا 25 درصد از اسیدهای موجود در صنایع غذایی را این اسید و نمک های آن تشکیل می دهند. کاربرد اصلی این ماده در نوشیدنی ها به ویژه نوشابه ها، ایجاد طعم خاص برای آنها است. اسید فسفریک در نوشابه در گرید خوراکی بیشترین استفاده را دارد.

این ترکیب در نوشابه و محصولات شیرین از رشد کپک ها و باکتری ها جلوگیری می کند. در واقع بیشتر خاصیت اسیدیته نوشابه ها، ناشی از حضور این ماده است. این ماده ی شیمیایی به صورت مستقیم بر تراکم استخوان پایین در زنان تاثیر گذار است و برطبق تحقیقات این ماده می تواند در جذب کلسیم تداخل ایجاد کند و باعث از بین رفتن آن شود.
کاربرد های صنعتی :
استفاده های صنعتی از این محصول در موارد متعددی همچون تولید کود کشاورزی، شوینده ها، محصولات آرایشی و بهداشتی و… می باشد.
- فسفات ها به طور گسترده در زیست شناسی به عنوان قندهای فسفریله شده مانند DNA ، RNA و ATP یافت می شوند.
- متافسفریک اسید و آنیدرید فسفریک یک نوع از این اسید بدون آب است و به عنوان جذب کننده رطوبت و خشک کننده استفاده می شود.
- از این اسید برای واکنش با هالیدهای مختلف برای تشکیل گاز هالید هیدروژن مانند HCl و HI استفاده می شود.
- به عنوان ماده ضد زنگ و برای اسید شویی استفاده می شود
- به طور گسترده در دندانپزشکی به عنوان سفید کننده دندان و جرم گیر برای تمیز کردن سطح دندان ها استفاده می شود.
- این ماده، واسطه ای شیمیایی در تولید خوراک های کشاورزی، واکس ها، جلا دهنده ها، صابون ها و مواد شوینده است.
- برای تنظیم pH در محصولات آرایشی و بهداشتی و مراقبت از پوست استفاده می شود
- استفاده به عنوان الکترولیت در پیل های سوختی
- افزودنی به آب مقطر به عنوان الکترولیت در ژنراتورهای اکسی هیدروژن
- به عنوان جز فاز متحرک در کروماتوگرافی مایع با عملکرد بالا
همچنین به عنوان عامل اکسید کننده شیمیایی برای تولید کربن فعال (فرآیند Wentworth) استفاده می شود.
کاربرد خرید اسید فسفریک در کشاورزی
کود اسید فسفریک یک ماده موثر برای رشد گیاهان استفاده است. این ماده شیمیایی از گیاه در برابر آلودگی های قارچی و کپکی جلوگیری می کند. این ماده شیمیایی در گیاهان شکسته و تجزیه نمی شود ولی میزان مصرف آن باید کنترل شود.
اسید فسفریک برای پسته:
کمبود فسفر در خاک، سرعت رشد درختان پسته را کاهش می دهند و برگ های سبز را تیره تر نشان می دهد. به همین دلیل برای جلوگیری از این عوارض، لازم است فسفر مورد نیاز را در اختیار درختان پسته قرار دهیم. کشاورزان این عنصر را در قالب کود به خاک اعمال می کنند. همانطور که می دانید این اسید یکی از منابع عالی برای تامین فسفر است؛ اما نمی توان آن را در قالب کود به طور مستقیم به خاک افزود، زیرا ترکیبی بسیار خورنده است. به همین دلیل از این اسید در تولید سایر کودها مانند سوپر فسفات تریپل بهره می برند.
بازار جهانی خرید اسید فسفریک
بر اساس مطالعه تحقیقاتی ، بازار جهانی خرید فسفریک اسید در سال 2019 حدود 45/85 میلیارد دلار تخمین زده شد و انتظار می رود این رقم تا سال 2026 به 60 میلیارد دلار برسد. پیش بینی می شود میزان خرید این محصول با رشد ترکیبی سالانه (CAGR) 3/7% از سال 2020 تا 2027 رشد کند. گستردگی کاربرد این محصول در مواردی همچون تولید کودهای فسفاته ، مانند مونو آمونیوم فسفات (MAP) و دی آمونیوم فسفات (DAP) ، سطح تقاضا برای این اسید را افزایش داده است. در سطح جهانی ، این اسید بعد از اسید سولفوریک ، دومین اسید معدنی محسوب می شود. این ماده در سه غلظت متفاوت جهت استفاده های متفاوت تولید می شود.
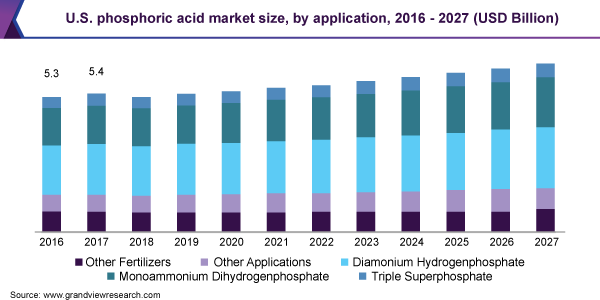
بررسی بازار منطقه ای:
آسیا و اقیانوسیه در سال 2019 بزرگترین بازار خرید این ماده را داشته است که این مقدار بیش از 48% بوده است. تخمین زده می شود این منطقه به دلیل ذخایر بالای سنگ فسفات در چین، که همچنین تولید کننده عمده آن است، موقعیت غالب خود را در طول سالهای پیش بینی حفظ کند. این کشور همچنین دارای تولید زیاد کودهای فسفاته و فسفر زرد است. با این حال، در سال های اخیر چین به دلیل مقررات دقیق در استفاده از کودهای فسفاته شاهد کاهش تقاضای محصول بوده است.
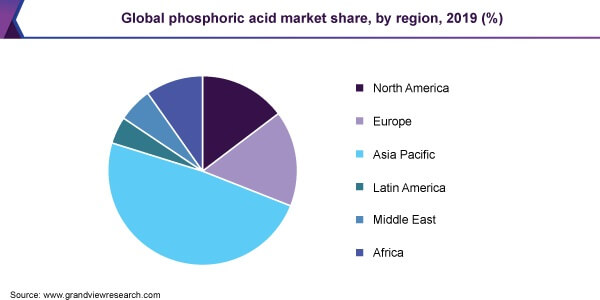
Aditya Birla Grasun Chemicals Limited (ABGCL) پیشرو در تولید اسید فسفریک خوراکی است که به طور گسترده ای توسط فرآیند حرارتی تولید می شود. پیش بینی می شود تغییر سبک زندگی و رشد اقتصادی بازار محصولات غذایی بسته بندی شده را تغییر دهد و تقاضای phosphoric acid درجه یک افزایش دهد. علاوه بر این ، از نظر حجم ، پیش بینی می شود که APAC و کشورهای آفریقایی رشد قابل توجهی را به دلیل افزایش تقاضای غذا منعکس کنند. آفریقای جنوبی یکی از بازارهای کلیدی این محصول در منطقه آفریقا است ، زیرا مشاهده می شود که این کشور به دلیل نوسانات شرایط جوی با تلاطم در تولید محصولات مواجه است.
MSDS و خطرات اسید فسفریک
این ترکیب جزو مواد خورنده است و در برخورد با پوست و چشم منجر به آسیب و سوختگی می شود اما اشتعال پذیر نیست. در هنگام استفاده از آن باید از روپوش، دستکش و عینک استفاده شود. همچنین از نگهداری آن در کنار مواد اکسید کننده و بازها خودداری شود.
| خطر آتش سوزی | غیر قابل اشتعال |
| استنشاق | تحریک دستگاه تنفسی و مسمومیت |
| پوست و چشم | آسیب جدی به پوست و ایجاد قرمزی و درد و سوختگی |
| بلع و گوارش | آسیب جدی به دستگاه گوارش، امکان سوراخ شدن مری و معده |
سوالات متداول
آیا فسفریک اسید برای انسان ها مضر است؟
این ماده باعث تحریک ریه، سرفه و تنگی نفس می شود. همچنین تماس آن با پوست خشکی و سوختگی آن ناحیه را به دنبال دارد.
آیا فسفریک اسید برای دندان ها مضر است؟
این ترکیب دارای خاصیت خورندگی بالایی برای دندان هاست، از این رو حتی مقدار کم آن در نوشابه ها نیز برای دندان ها مضر است.
کاربرد اسید فسفریک در محصولات لبنی چیست؟
نمک این اسید در بسیاری از محصولات لبنی یافت می شود و باعث افزایش کیفیت و ماندگارای این محصولات می شود. این ترکیب در غذاها می تواند PH را تنظیم کند.
جایگزین اسید فسفریک چیست؟
برخی از اسید های آلی رایج شامل اسید سیتریک، استیک اسید و فرمیک اسید جایگزین های این ترکیب هستند.
آیا حضور فسفریک اسید در غذاها ایمن است؟
این اسید بر طبق نظریه سازمان غذا و دارو ترکیبی ایمن به حساب می آید و در بسیاری از محصولات غذایی و نوشیدنی ها حضور دارد.








![دی بوتیل هیدروکسی تولوئن [هیدروکسی تولوئن بوتیل دار شده(BHT)]](https://www.mbkchemical.com/wp-content/uploads/2024/02/afff926caa0ffa78b7033e209451d176-300x300-1.jpg)





نقد و بررسیها
هنوز بررسیای ثبت نشده است.