توضیحات
سدیم دی کرومات نارنجی تا قرمز رنگ می باشد، بلورین و غیر آلی است وپس از حرارت دادن موجب انتشار ذرات سمی کروم می شود. برای خرید فروش دی کرومات سدیم و همچنین جهت کسب اطلاع از قیمت ها و چگونگی ثبت سفارش این محصول با مشاوران ما در موسسه مبتکران شیمی در ارتباط باشید.
خرید سدیم دی کرومات :
در حال حاضر موسسه ی مبتکران شیمی به عنوان یکی از تامین کنندگان محصولات شیمیایی کشور, طیف گسترده ای از مواد شیمیایی آزمایشگاهی و صنعتی را از برندهای معتبر در اختیار تولید کنندگان قرار می دهد. برای کسب اطلاعات بیشتر می توانید با همکاران ما در ارتباط باشید.
فروش سدیم دی کرومات :
جهت اطلاع از نحوه ی فروش این محصول و ثبت سفارش شما می توانید با همکاران ما در واحد فروش موسسه مبتکران شیمی در در ارتباط باشید.
قیمت سدیم دی کرومات :
برای آگاهی از قیمت با کارشناسان فروش ما در ارتباط باشید.
مشخصات فیزیکی شیمیایی
این ترکیب خاصیت خورندگی بالایی دارد و یک عامل اکسید کننده ی قوی به حساب می آید. از کاربرد های اصلی آن می توان به استفاده در تولید سایر ترکیبات شیمیایی کروم نظیر کرومات پتاسیم، دی کرومات امونیوم، اسید کرومیک، استات کرومیک، کلرید کرومیک، سولفات کروم و… اشاره نمود. از کاربرد های دیگر این ماده استفاده در گل های حفاری، پردازش فلزات، نگهدارنده های چوب، تولید رنگ ها و مواد شیمیایی آلی و همچنین مهار کننده ی خوردگی می باشد.
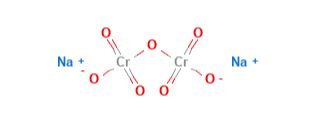
ساختار مولکولی آن به صورت زیر است:
خواص فیزیکی این ماده به شرح زیر می باشد
| فرمول شیمیایی | Na2Cr2O7 |
| جرم مولکولی | 261.97 g/mol |
| نقطه ی ذوب | 356.7 درجه سانتی گراد |
| دانسیته | 2.52 g/cm3 |
فرم دهیدراته ی رایج آن Na2Cr2O7·2H2O با وزن مولکولی 2.52 می باشد. نقطه ی ذوب آن 375 درجه ی سانتی گراد است و در 400 درجه ی سانتی گراد تجزیه می شود. در اثر حرارت به مدت طولانی در دمای 100 درجه سانتی گراد دو مولکول آب خود را از دست می دهد. این ماده در آب به راحتی حل می گردد اما در الکل ها حلالیت کمی دارد
سدیم دی کرومات به خصوص در واکنش پذیری و خواص فیزیکی بسیار شبیه به پتاسیم دی کرومات است اما نوع سدیم آن بسیار در آب محلول پذیر تر می باشد اما وزن اکی والان کمتری دارد.
تولید و واکنش ها
ماده ی اولیه ی خام جهت تولید محصول فوق سنگ معدن کرومیت می باشد که درصد ترکیبات آن به قرار زیر است:
| نام ماده | فرمول شیمیایی | درصد ترکیب |
| اکسید کروم | Cr2O3 | 45% |
| آهن | Fe | 9% |
| اکسید آلومینیوم | Al2O3 | 6% |
| اکسید منیزیم | MgO | 10-20% |
| اکسید کلسیم | CaO | 0.15% |
سدیم بی کرومات از واکنش اسید سولفوریک با کرومات سدیم که به وسیله ی تکلیس مخلوط سنگ معدن کرومیت ، سنگ آهک و سودااش به دست آمده است تولید می گردد.
کرومیت یا سنگ آهن-کروم FeCr2O4 به صورت مرغوب حاوی حدود 50 درصد اکسید کروم Cr2O3 است و معمولا از معادن کشور هندوستان و یا جنوب غرب آمریکا استخراج می گردد. این سنگ معدن را توسط دستگاه های آسیاب گلوله ای خرد و به ذرات کاملا ریز در می آورند به طوری که 91-98 درصد از ذرات آن اندازه ای در حدود 150 الی 200 میکرون پیدا کنند. سپس آن را با حداقل 90 درصد سودااش و مقادیر مختلفی آهک مخلوط می کنند.
پس از آن مخلوط را در دستگاه مخلوط کن دوار کاملا مخلوط نموده و در کوره ی دوار تکلیس (2000-2100 درجه فارنهایت) قرار می دهند. آهک در اینجا ماده ی گدازنده جهت سرعت جریان به کار می رود. پس از 4 ساعت مواد گداخته و سرخ شده در کوره را مستقیما به مخازن شست و شو جهت تصفیه و یا مخازن غلظت دهنده می فرستند تا در آنجا کرومات محلول در آب داغ و غلیظ گردد.. محلول به دست آمده از آخرین سینی موجود در مخزن غلظت دهنده را فیلتر می کنند، سپس پسمانده را توسط خشک کن های دوار خشک می کنند. سپس مایع اصلی حاصل از فیلتر را به مخزن شست و شو و یا غلظت دهنده بر می گردانند.
-
جداسازی آلومینا
محلول سرریز شده از مخزن شست و شو را فیلتر می کنند و به دستگاه هیدرولیز منتقل می نمایند. در اینجا آلومینات سدیم هیدرولیز شده و به وسیله ی افزایش آهسته ی محلول dichromate sodium ، به صورت اکسید آلومینیوم نامحلول در می آید. واکنش آن به شرح زیر است:
2NaAlO2+9H2O-> Al2OH2O+2NaOH
2NaOH+Na2Cr2O7-> 2Na2Cr2O4+H2O
افزودن محلول بی کرومات سدیم بایستی دقیقا با احتیاط انجام پذیرد تا به جای ایجاد ترکیب ژلاتینی ، هیدرات آلومینای قابل فیلتر به دست آید. بعد از جدا کردن آلومینا ، استفاده از محلول کرومات به دست آمده بستگی به محصول مورد نظر دارد.
-
کاهش pH
کرومات سدیم را از مخزن ذخیره سازی به داخل مخزن اسیدی کننده انتقال می دهند تا در آنجا با افزودن سولفوریک اسیدpH از 8.04 به 4.7 کاهش یابد. کرومات به دی کرومات تبدیل می شود و در نتیجه سولفات سدیم تشکیل می گردد. بیشتر سولفات سدیم بلوری شده از محلول جوش، به صورت سولفات سدیم بدون آب خارج می سازند. بلور ها را به وسیله ی فیلتر کردن جدا می کنند و محلول فیلتر شده را به داخل تبخیر کننده های سه گانه می ریزند تا باقی مانده ی سولفات نیز بلورین و متبلور شوند.
-
تبلور
محلول داغ و شفاف دی کرومات اشباع شده را به آب خنک شده ی بلور ساز تغذیه می کنند. تقریبا 70 درصد دی کرومات سدیم متبلور می شود و آن را به وسیله ی تداوم عمل سانتریفیوژ جدا و خارج می نمایند.مایع اصلی را دوباره به دستگاه تبخیر کننده برگشت می دهند. پس از خشک کردن به وسیله ی خشک کن ها ، بلور های قرمز dichromate sodium را بسته بندی می کنند.
بی کرومات سدیم ممکن است به وسیله ی تبلور مجدد از آب، خالص گردد. سولفات سدیمی که به وسیله ی شست و شو به دست آمده است را توسط خشک کن دوار خشک می کنند. این محصول فرعی که به عنوان کیک نمک کروم فروخته می شود جهت صنایع کاغذ سازی به کار می رود
واکنش های تولید سدیم دی کرومات:
4FeCr2O4+8Na2CO3+7O2-> 8Na2CrO4+2Fe2O3+8CO2
2Na2CrO4+H2SO4-> Na2Cr2O7+Na2SO4+H2O
دی اکسید کربن تحت فشار را می توان در تغییر و تبدیل کرومات به دی کرومات، جانشین اسید سولفوریک نمود که در این حالت بیکربنات سدیم به عنوان یک محصول فرعی به جای سولفات سدیم به دست می آید.
کاربرد های سدیم دی کرومات
ترکیب فوق میلیون ها کیلوگرم در سال تولید می گردد و صرف مصارف گوناگونی می شود. چین یکی از تولید کنندگان اصلی این ماده ی شیمیایی است با این حال کارخانه های تولید کننده ی چینی سرعت تولید پایین تری ( کمتر از 50,000 تن در هر سال در هر کارخانه) نسبت به کارخانه های قزاقستانی دارند (بیش از 100,000 تن در هر سال). کارخانه های تولیدی در آمریکا، روسیه و بریتانیا میزان تولید متوسطی بین 50,000 -100,000تن در سال دارند.
به غیر از اهمیت این ترکیب در تولید سایر محصولات کروم از آن در صنایع گوناگونی نظیر گالوانیزاسیون، آبکاری، پردازش چرم و… استفاده می نمایند.
فلزکاری:
سدیم بی کرومات در این صنعت موجب جلوگیری از خوردگی می شود. تمیز شدن فلزات را آسانتر می کند و چسبندگی رنگ به سطح را بهبود می بخشد.
محصولات ارگانیک:
به عنوان اکسید کننده در تولید ویتامین K و موم ها استفاده دارد.
رنگدانه ها:
برای تولید رنگدانه های غیر آلی این ترکیب مورد استفاده قرار می گیرد و طیف وسیعی از رنگ های پایدار را تولید می کند. برخی از گرید های خاص کرومات به عنوان عامل ضد خوردگی در زیر لایه ها نیز مورد استفاده قرار می گیرد.
-
انواع رنگدانه ها
+ رنگدانه ی زرد کروم : این رنگدانه زرد روشن است که شهرت خاص خود را دارد.در انواع سایه ها از زرد باز مایل به سبز روشن گرفته تا زرد مایل به قرمز تیره یافت می شود. رنگ های زرد کروم قدرت پوشش خوبی دارند و پراکنده شدن آن ها به سادگی صورت می گیرد.
+ سبز کروم: سبز کروم به خاطر درخشندگی، دوام، قدرت پوشش و قیمت پایین برای مدت ها رنگدان ه ای پرمصرف بود. در درجات رنگ مختلفی از سبز روشن مایل به زرد تا سبز تیره مایل به آبی این نوع رنگدانه مشاهده می شود. سبز کروم مقاومت قلیایی ضعیفی دارد و در رنگ های لاتکس به کار نمی رود.
+ روی کرومات بازی: خواص این رنگدانه تا حدودی شبیه خواص زرد روی است رنگ آن زرد مایل به سبز بوده و برای آماده کردن سطح فلزاتی مانند فولاد و آلومینیوم به کار می رود و موجب می شود تا قدرت آن ها در ارتباط با چسبندگی و مقاومت در برابر خوردگی بالا رود.
+ سبز اکسید کروم: این رنگدانه سبز نسبتا تیره می باشد. دوام و مقاومت عالی دارد . قدرت پوششی متوسطی داشته و امولوسیون کردن آن آسان است. با بازتابش مادون قرمز بالایی که دارد رنگدانه ی سبز مهمی در رنگ های استتاری است.
+ نارنجی کروم: این رنگدانه به دلیل بالا بودن قیمت، کمتر مورد استفاده قرار می گیرد و بیشتر از نارنجی مولیبدات استفاده می نمایند.
+ سرب سیلیکو کرومات بازی: این رنگدانه نیز نارنجی روشن است که ابتدا به عنوان رنگدانه ی ضد زنگ در ساختمان های فولادی به کار می رفت. به خاطر قدرت پوششی ضعیف می توان آن را با سایر رنگدانه ها مخلوط کرد تا رویه هایی با فام های مختلف که همچنان دارای خواص ضد زنگ می باشند به دست آید.
نساجی:
سدیم دی کرومات به عنوان یک افزودنی به رنگ های اسیدی برای افزایش سرعت و بهبود خواص رنگ آمیزی افزوده می شود.
سرامیک:
این ماده شیمیایی در تولید شیشه های رنگی و لعاب های سرامیکی مورد استفاده قرار می گیرد.
سنتز مواد آلی:
در سنتز مواد آلی سدیم دی کرومات به عنوان یک اکسید کننده در واکنش های کاهشی در حضور اسید سولفوریک مورد استفاده قرار می گیرد که نمونه هایی از آن در زیر ذکر شده اند :
- در اکسیداسیون P- نیتروتولوئن برای تشکیل P- نیترو بنزوئیک اسید،
- اکسیداسیون سیکلوهگزان برای تشکیل سیکلوهگزانول
- در شکل گیری آدیپیک اسید
- در اکسیداسیون نرمال بوتانول برای تشکیل n- بوتیل آلدهید
ایمنی:
بی کرومات سدیم در صورت حرارت دادن گاز های سمی متساعد می کند. در شکل زیر بخشی از ایمنی این محصول را می توانید مشاهده نمایید
منبع:
- کتاب طرح های کوچک شیمیایی سودبخش ترجمه و تالیف احمد مومن هروی
- کتاب فرهنگ رنگ ترجمه دکتر ابراهیم بیگدلی و دکتر محسن قلمکار معظم و فرانک منطقی
















نقد و بررسیها
هنوز بررسیای ثبت نشده است.