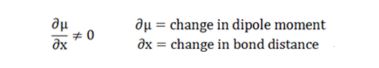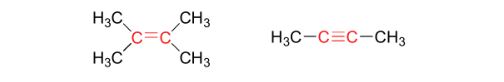FTIR چیست ؟ اسپکترومتری مادون قرمز تبدیل فوریه (Fourier Transform Infrared Spectrometer) که صورت مخفف آنالیز FTIR نامیده می شود به صورت عمده در سنتز مواد آلی، پلیمر ها، علوم شیمی و مهندسی شیمی، صنعت تولید دارو، تجزیه و تحلیل مواد غذایی و… مورد استفاده قرار می گیرد. همچنین با توجه به اینکه امکان اتصال این دستگاه به تکنیک های کروماتوگرافی وجود دارد می توان مکانیسم واکنش های شیمیایی و تشخیص مواد ناپایدار با چنین ابزاری را مورد بررسی قرار داد.
FTIR تکنیکی شیمیایی است که برای شناسایی گروه های عاملی از آن استفاده می کنند. این تکنیک می تواند میزان شدت طیف مادون قرمز را بر اساس طول موج جذبی رسم نماید.
بر اساس مقدار طول موج می توان نور مادون قرمز را به سه دسته ی زیر تقسیم بندی نمود.
- مادون قرمز دور (4 ~ 400cm‐1)
- نزدیک (4,000 ~ 14,000cm‐1 )
- مادون قرمز متوسط (400 ~ 4,000cm‐1)
ارتعاشات
کشف نور مادون قرمز به قرن نوزدهم بر می گردد. و از آن زمان تا کنون دانشمندان راهای گوناگونی برای استفاده از این نور پیدا کرده اند. طیف سنجی مادون قرمز روشی است که دانشمندان برای تعیین ساختار مولکول ها با کمک جذب اشعه ی مادون قرمز استفاده می کنند.طیف مادون قرمز طیف ارتعاش مولکولی است زیرا پیوند های موجود در مولکول بعد از جذب نور مادون قرمز شروع به ارتعاش می نمایند و در صورت فعال بودن دچار تغییر ممان دو قطبی می گردند
این ارتعاشات را می توان به2 مورد کلی زیر تقسیم بندی نمود
- کششی (متقارن و نامتقارن)
- خمشی (4 دسته)
برای یافتن اینکه مولکولی با داشتن N اتم چند حالت ارتعاشی نیز دارد از فرمول زیر استفاده می نمایند:
| مولکول خطی | 3N-5 ( مولکول خطی فاقد چرخش است) |
| مولکول غیر خطی | 3N-6 (همه ی احتمالات ارتعاش وجود دارد) |
اما همه ی گروه های عاملی در مادون قرمز پیک نمی دهند
پس برای آنالیز کدام مواد از FTIR می توان استفاده نمود؟
بعضی پیوند ها مادون قرمز را بسیار بیشتر از سایر پیوند ها جذب می نمایند(فعال) و برخی پیوند های دیگر نیز کلا این نور را جذب نمی نمایند (غیر فعال). به منظور جذب اشعه ی مادون قرمز در حالت ارتعاشی باید شاهد تغییر دوره ای ممان دو قطبی در مولکول باشیم. اینگونه ارتعاشات را اصطلاحا فعال مادون قرمز می نامند. به طور کلی قطبی تر بودن گروه عاملی موجب جذب بیشتر این اشعه می شود. به عنوان مثال گروه کربونیل بسیار قطبی است و جذب بالایی از خود نشان می دهد. اما پیوند کربن- کربن 3 گانه در بیشتر ساختارهای آلکینی کمتر قطبی است .
بنابراین ارتعاش کششی موجود سبب تغییرات زیادی در ممان دو قطبی مولکول نمی شود. گروه های آلکیلی نیز جذب نسبتا ضعیفی نسبت به کربونیل دارند HCl و CO2 نمونه های فعال مادون قرمز می باشند
همانطور که گفته شد ممان دو قطبی در آنالیز های مادون قرمز نقش اساسی دارد. عملا مولکول باید بعد از جذب نور بتواند دچار تغییر ممان دو قطبی شود تا در اینگونه آنالیز ها پیک دهد. مولکول های با پیوند کششی متقارن دارای ممان دوقطبی 0 و غیر فعال در آنالیز FTIR می باشند
نمونه ای از این مولکول ها را در شکل زیر می توانید مشاهده کنید
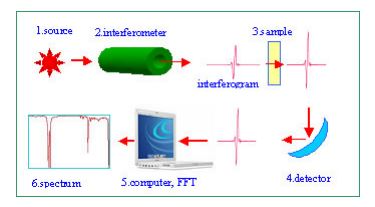
این آنالیز چگونه کار می کند؟
در این فرایند اشعه ی مادون قرمز با 100 الی 10000 cm-1 به نمونه تابیده می شود. برخی از این اشعه ها جذب و برخی دیگر از نمونه عبور می کنند. اشعه های جذب شده ، توسط مولکول های نمونه به انرژی چرخشی و ارتعاشی تبدیل می شوند. در نهایت سیگنال های نهایی توسط آشکار ساز در دامنه ی 400 الی 4000cm-1 نمایش داده می شوند. لازم به ذکر است هر مولکول طیف های مربوط به خود را نشان می دهد و اصطلاحا طیف اثر انگشتی مربوط به خود را دارد. در نتیجه با توجه به طیف های اثر انگشتی که مختص به هر مولکول می باشند شناسایی با کمک این آنالیز بسیار آسان می گردد.
اما چگونه این طیف ها رسم می شوند؟
آنالیز FT-IR می تواند ارتعاشات موجود در گروه های عاملی یک نمونه را شناسایی کند. به طور کلی وقتی که نور به این گروه های عاملی برخورد می کند پیوند های شیمیایی موجود کش می آیند و یا خم می گردند. در نتیجه گروه شیمیایی موجود در نمونه (بدون در نظر گرفتن ساختار بقیه ی مولکول) تمایل به جذب اشعه ی مادون قرمز در طیف خاصی از طول موج را دارد. به عنوان مثال پیوند کششی C=O گروه کربونیل در مولکول های مختالف در محدوده ی 1700cm‐1 ظاهر می شود. در نتیجه براساس رابطه ی بین موقعیت طول موج و ساختار شیمیایی می توان شناسایی گروه های مختلف عاملی موجود در نمونه را به راحتی انجام داد .
موقعیت گروه های عاملی تقریبا می توان گفت که همیشه ثابت است و با تغییراتی مانند دما، فشار، نمونه برداری، تغییر ساختار مولکول و…سازگار می باشند
مزایا و معایب:
طیف سنجی مادون قرمز همانند سایر روش های دستگاهی برای بعضی از نمونه ها خوب عمل می کند و در سایر موارد نیز ضعیف عمل می نماید. برخی از مزایا و معایب طیف سنجی مادون قرمز در جدول زیر آورده شده است. با شناخت از مرایا و معایب این تکنیک می توان آن را در موارد مناسب به کار برد
| مزایا | معایب |
| جامدات، مایعات ، گاز ها ، نیمه جامدات، پودر ها، پلیمر ها همه با کمک این تکنیک قابل آنالیز می باشند | اتم ها یا یون ها طیف مادون قرمز ندارند |
| موقعیت، شدت و پهنای پیک همه اطلاعات مفیدی درباره ی نوع گروه عاملی به ما می دهند | مولکول های قطبی و یا دوتایی مانند Cl2و Br2و… طیف مادون قرمز ندارند |
| سریع، آسان، ارزان و حساس است (حتی مقدار میکروگرم از ماده را می تواند تشخیص دهد) | ترکیبات پیچیده و محلول های آبی تجزیه و تحلیل پیچیده ای در آنالیز مادون قرمز دارند |
چرا هر گروه عاملی در طول موج خاصی پیک می دهد؟
طبق فرمول های بالا دو عامل می تواند بر روی فرکانس و طول موج تاثیر داشته باشد. اولین عامل ثابت نیروی پیوندی (K) و دومی جرم کاهش یافته می باشد. طبق فرمول جرم کاهش یافته (M1M2)/(M1+M2) است که در آن M1و M2 جرم اتمی هستند. هیچ دو ماده ای در جهان نمی توان یافت که دارای جرم های یکسان و ثابت نیروی پیوندی یکسان نیز باشند به همین دلیل طیف مادون قرمز هر ماده شیمیایی منحصر به فرد است.
بیشتر بخوانید: طیف سنجی جرمی چیست ؟
برای یافتن اینکه کدام گروه عاملی در کدام طول موج پیک می دهد جدول ها و دیتابیس های زیادی وجود دارد که با مراجعه به آن ها می توان موقعیت مربوط به هر کدام را مشاهده نمود
برای درک بهتر این مطلب به مثال زیر توجه نمایید:
-
جرم کاهش یافته
| پیوند | پیک پیوند کششی CH بر حسب Cm-1 |
| C-H | ~3000 |
| C-D | ~2120 |
C-H و C-D دارای نیروی پیوند یکسان هستند اما جرم کاهش یافته ی متفاوتی دارند. با دو برابر شدن جرم هیدروژن موقعیت پیک به حدود 800cm-1 کاهش یافته است ( رابطه ی عکس میان جرم کاهش یافته و طول موج)
-
ثابت نیرو
| پیوند | پیک پیوند کششی CH بر حسب Cm-1 |
| C-H | ~3000 |
| H-C=O | ~2750 |
هنگامی که هیدروژن به گروه C=O متصل می گرددموقعیت پیوند کششی C-Hبه ~2750cm-1 کاهش پیدا میکند این دو پیوند C-H هر دو دارای جرم کاهش یافته ی یکسان اما ثابت نیروی متفاوتی هستند . اکسیژن موجود در مولکول دوم چگالی الکترون را از پیوند C-Hدور می کند. بنابراین موجب ضعیف شدن و کاهش ثابت نیرو می شود. همین امر کاهش ~250cm-1 در پیوند C-H متصل شده به اکسیژن را سبب می گردد.
همچنین ثابت نیرو در پیوند ها به ترتیب زیر است
پیوند سه گانه>پیوند دو گانه> پیوند یگانه
محور عمودی در FTIR نشانه ی چیست؟
همانطور که پیش از این نیز مشاهده شد نمودار افقی در آنالیز FTIR مربوط به طول موج گروه عاملی و نمودار عمودی مربوط به شدت جذب گروه های عاملی است
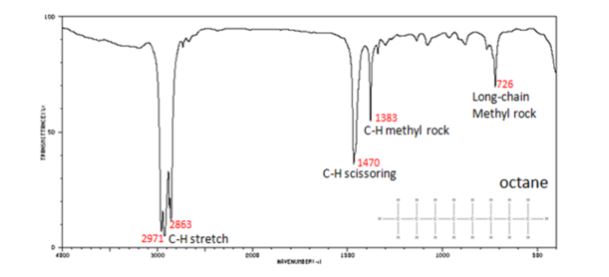
ارتعاش های مختلف گروه های عاملی در مولکول موجب شدت های متفاوت می شود. زیرا ∂μ∂/x برای هر ارتعاش متفاوت است. برای درک بهتر به طیف مولکولی که در زیر رسم شده است دقت کنید:
بیشترین شدت مشاهده شده در گروه عاملی C-H موجود، مربوط به اکتان در 2971و 2863 cm-1 است.
ضعیف ترین طیف مشاهده شده نیز در مولکول اکتان مربوط به پیوند بلند زنجیر کربن-کربن اکتان در 726cm-1 می باشد.
تفاوت این دو به دلیل شدت تغییرات ممان دو قطبی است. در پیوند C-H تغییرات ممان دو قطبی در اثر ارتعاشات کششی بسیار بیشتر از ارتعاشات لرزشی به وجود آمده در پیوند C-C بوده است.
شدت کششی>شدت خمشی
یکی از موارد دیگری که شدت جذب را تعیین می نماید غلظت مولکول در نمونه است ( قاونون بیر-لامبرت) که به ∂μ∂/x وابسته می باشد
جذب یک اندازه ی مطلق از میزان جذب اشعه ی مادون قرمز برای یک مولکول خاص در طول موجی مشخص می باشد. برای یک نمونه ی خالص غلظت در ماکزیموم ترین حالت ممکن به سر می برد و شدت پیک نشان دهنده ی مقدار ∂μ∂/x برای ارتعاشات مختلف است.
بنابراین در یک مخلوط مولکول ها می توانند پیک هایی با شدت های مختلف داشته باشند زیرا مولکول هایی هستند که با غلظت های مختلفی در نمونه حضور دارند
پهنای پیک
به طور کلی عرض هر کدام از پیک ها برای نمونه های جامد و مایع به محیط شیمیایی آن ها بستگی دارد. که همین امر خود نیز به مقاومت بین مولکولی پیوند ها مانند پیوند هیدروژنی وابسته است. به عنوان مثال پیوند هیدروژنی در مولکول آب با خود مولکول آب در محیط های شیمیایی متفاوتی قرار دارند . به خاطر اینکه تعداد و قدرت پیوند هیدروژنی با محیط شیمیایی متفاوت است ، ثابت نیرو متفاوت خواهد بود و در طول موج های متفاوتی با توجه به جذب نور مادون قرمز توسط مولکول پیک می دهد
در نمونه هایی که پیوند هیدروژنی حضور دارد تعداد و نیروهای بین مولکولی در نمونه بسیار بیشتر است و موجب پهن تر شدن پیک می گردد
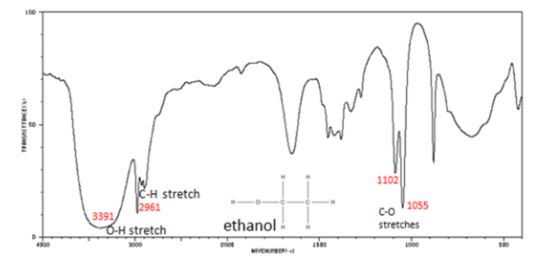
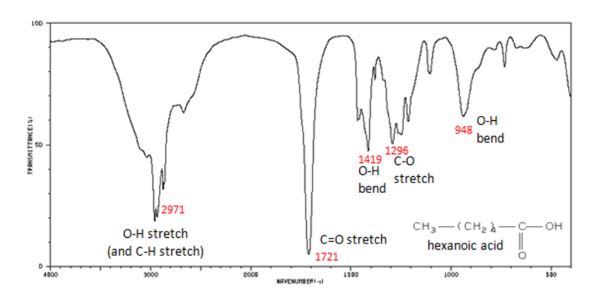
در طیف های FTIR زیر می توانید پیک های پهن موجود در اتانول و هگزانیک اسید را مشاهده نمایید
-
تحلیل نمودار اتانول
الکل ها با توجه به داشتن گروه های عاملی OH و CO در طول موج های مختلفی پیک می دهند
O-H کششی در 3500-3200 cm-1
C-O کششی در 1260-1050 cm-1
C-H کششی 2961 cm-1
همچنین وجود پیک های پهن در آن به دلیل وجود پیوند های هیدروژنی بین مولکولی می باشد
-
تحلیل هگزانوئیک اسید
O-H کششی در 3300-2500 cm-1
C=O در 1760-1690 cm-1
C-O در 1320-1210 cm-1
O-H در 1440-1395 و 950-910 cm-1
با توجه به شکل گروه عاملی C=O به صورت پهن در بازه ی 1760-1690 cm-1 پیک می دهد. مکان دقیق پیک پهن C=O به اشباع بودن و یا نبودن کربوکسیلیک اسید، دیمر شدن و یا داشتن پیوند هیدروژنی وابسته است.
کاربرد ها
شرکت های تولید کننده ی مواد برای بررسی کنترل کیفیت محصولات خود از آنالیز FTIR استفاده می نمایند. تکنیک فوق می تواند هر گونه ناخالصی موجود در نمونه را شناسایی کند. با شناسایی ناخالصی می توان منشا آن را پیش بینی نمود و آن را حذف کرد. از آنجایی که هر مولکول پیک شناسایی مخصوص به خود را دارد ، در نتیجه با دیدن پیک اضافه در آنالیز نمونه می توان به وجود ناخالصی و آلاینده در آن پی برد. معمولا این تکنیک برای شناسایی و آنالیز ذرات با 10 الی 50 میکرون مورد استفاده قرار می گیرد.
به طور کلی آنالیز FTIR در موارد زیر استفاده می گردد:
- شناسایی و تشخیص مواد ناشناخته
- شناسایی ناخالصی های موجود در نمونه
منبع:
Libretexts. (2019, June 03). 13.15: Some Vibrations Are Infrared Inactive. Retrieved July 16, 2019, from https://chem.libretexts.org/Bookshelves/Organic_Chemistry
/Map:_Organic_Chemistry_(Bruice)/13:_Mass_Spectrom
etry,_Infrared_Spectroscopy,_and_Ultraviolet//Visible_Spectroscopy
/13.15:_Some_Vibrations_Are_Infrared_Inactive
خرید و فروش مواد شیمیایی را به ما در مبتکران شیمی بسپارید