اکسیژن با نام دیگر Oxygen و نماد O2 عنصری غیر فلزی در گروه 16 ام جدول تناوبی می باشد. این عنصر گازی بی رنگ، بی بو و بی مزه است. در این مقاله با خواص این ترکیب ، چگونگی تولید، نوع مایع و ایزوتوپ ها ( نوع 18 و 17 و…) آشنا خواهیم شد. پس با ما همراه باشید.
این عنصر ماده ای ضروری برای جانداران به حساب می آید. موجودات زنده برای ادامه ی حیات به تنفس این گاز احتیاج دارند و آن را به دی اکسید کربن تبدیل می نمایند. گیاهان با جذب دی اکسید کربن و تبدیل آن به O2 سبب افزایش این گاز در اتمسفر می شوند.
این ماده در ترکیب با سایر مواد می تواند منجر به واکنش سوختن شود. این واکنش معمولا با آزاد سازی گرما و نور همراه می باشد. مهم ترین محصول حاصل از این فرایند آب است.
.
.
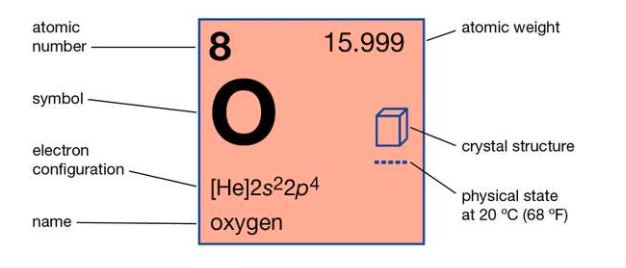
ویژگی های این عنصر را در جدول زیر می توانید مشاهده نمایید
| عدد اتمی | 8 |
| وزن اتمی | 15.9994 |
| نقطه ی ذوب | −218.4 °C |
| نقطه ی جوش | −183.0 °C |
تاریخچه
اکسیژن در حدود سال 1772 توسط یک شیمیدان سوئدی به نام کارل ویلهلم شل کشف شد. این شیمیدان با گرم کردن نیترات پتاسیم ، اکسید جیوه و بسیاری از مواد دیگر توانست منجر به کشف این عنصر مهم شود.
یک شیمیدان انگلیسی ، جوزف پریستلی نیز به طور مستقل اکسیژن را در سال 1774 با تجزیه حرارتی اکسید جیوه کشف کرد.
در سال های 1775-80 ، شیمیدان فرانسوی آنتوان لاوران لاووازییه نقش اکسیژن در تنفس و احتراق را تفسیر کرد و توانست نظریه فلوگوستون را که تا آن زمان پذیرفته شده بود ، تفسیر کند. این دانشمند تمایل این عنصر با ترکیب با سایر مواد و به وجود آوردن اسید های گوناگون را مورد بحث قرار داد و نام (oxygène ) به یونانی به معنی اسید سابق را برای این عنصر در نظر گرفت.
خصوصیات
نسبت اکسیژن بر حسب حجم در جو 21 درصد و از نظر وزن در آب دریا 89 درصد است. در سنگ ها این عنصر با فلزات و غیر فلزات ترکیب می شود و اکسید هایی به شکل اسیدی (مانند گوگرد ، کربن ، آلومینیوم و فسفر) یا بازی (مانند کلسیم ، منیزیم و آهن) و یا ترکیبات نمکی تشکیل می دهد. لازم به ذکر است که این ترکیبات منابعی برای اکسیژن به حساب نمی آیند زیرا جداسازی این عنصر از ترکیبات مذکور بسیار گران قیمت می باشد.
- در دمای -183 درجه ی سانتی گراد این عنصر به صورت مایع و به رنگ آبی کم رنگ دیده می شود.
- در دمای حدود 218 درجه ی سانتی گراد این ماده جامد است.
- اکسیژن خالص 1.1 برابر سنگین تر از هوا است.
- تمام اکسیژن آزاد موجود در جو به دلیل فتوسنتز گیاهان است.
- 3 پارت از این عنصر در 100 پارت از آب در دمای 20 درجه ی سانتی گراد حل می گردد. انحلال این ماده در آب دریا کمتر است.
- این ماده به صورت محلول برای تنفس ماهی و سایر موجودات دریایی ضروری است.
اکسیژن مایع چیست؟
این ماده جز مایعات کرایوژنیک قرار می گیرد. مایعات کریوژنیک گازهای مایعی هستند که دمای جوش آنها در زیر دمای -130 درجه فارنهایت قرار دارد. اکسیژن مایع دارای نقطه جوش -297 درجه فارنهایت است (183 درجه سانتیگراد) می باشد. در نتیجه جز این دسته بندی قرار می گیرد. این مایع به صورت آبی کم رنگ می باشد و برای ذخیره سازی نیاز به ظروف عایق دارد.
در شکل مایع ، اکسیژن بسیار فشرده شده است. این بدان معنی است که یک لیتر برابر با 860 لیتر از این گاز است.
به دلیل حمل آسانتر این ماده در فرم مایع برای درمان بیمارانی که تحت درمان با این گاز قرار دارند بیشتر مورد استفاده قرار می گیرد
ایزوتوپ ها
اکسیژن طبیعی ترکیبی از سه ایزوتوپ پایدار است: اکسیژن 16 (99.759 درصد) ، اکسیژن 17 (0.037 درصد) و اکسیژن 18 (0.204 درصد).
چندین ایزوتوپ رادیواکتیو مصنوعی از این عنصر شناخته شده است که از این میان می توان به اکسیژن 15 با نیمه عمر 124 ثانیه اشاره نمود.
آلوتروپ ها
این عنصر دارای دو آلوتروپ دو اتمی O2 و سه اتمی (O3 گازی مرکب از سه اتم اکسیژن، با نام اوزن ) می باشد. اوزن می تواند طبق معادله ی زیر تولید شود:
3O2->2O3
فرایند فوق گرماگیر است و برای انجام این فرایند نیاز به اعمال انرژی می باشد. فرایند برگشتی این واکنش با کمک فلزات واسطه و یا اکسید های آن رخ می دهد
ازن یک اکسید کننده قوی است و قادر به تبدیل دی اکسید گوگرد به تری اکسید گوگرد ، سولفیدها به سولفات ها ، یدیدها به ید و بسیاری از ترکیبات آلی به مشتقات اکسیژنی آن ها مانند آلدهیدها و اسیدها می باشد.
در نتیجه استفاده از این ماده برای تبدیل هیدروکربن های منتشر شده از اگزوز خودرو ها به اسید و آلدهید ها می تواند بسیار مهم باشد و از آلودگی های منتشر شده توسط دود خودرو ها جلوگیری به عمل می آورد. ازن در صنعت به عنوان یک معرف شیمیایی ، ضد عفونی کننده در تصفیه آب و فاضلاب و سفید سازی پارچه در صنعت نساجی مورد استفاده قرار می گیرد
تولید:
روش های گوناگونی با بازده های مختلف برای آماده سازی و تولید این ماده وجود دارد. در ادامه با چند روش آزمایشگاهی تولید این ماده بیشتر آشنا می شویم:
- تجزیه حرارتی نمکهای خاصی مانند کلرات پتاسیم یا نیترات پتاسیم:
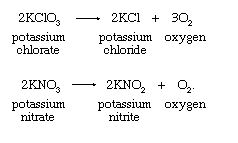
تجزیه ی حرارتی پتاسیم کلرید توسط اکسید های فلزات واسطه کاتالیز می شود.
منگنز دی اکسید (پیرولوزیت ، MnO2) اغلب به عنوان کاتالیزگر در این فرایند مورد استفاده قرار می گیرد. دمای مورد نیاز برای این فرایند با کمک کاتالیزور از حدود 400 درجه ی سانتی گراد به 250 درجه ی سانتی گراد کاهش می یابد
- تجزیه حرارتی اکیسد های فلزات سنگین
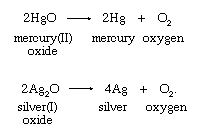
همانطور که پیش از این نیز گفته شد شیل و پریسلتی اکسیژن را طبق همین واکنش و با کمک اکسید جیوه سنتز نمودند.
- تجزیه حرارتی پراكسیدهای فلزی یا هیدروژن پراكسید:
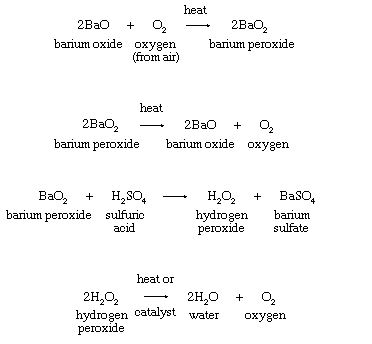
- الکترولیز آب، حاوی مقادیر اندک اسید و نمک برای افزایش هدایت و بهبود جریان الکتریکی
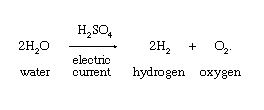
در صورتی که این ماده در مقیاس بالا و تناژ بالا مورد نیاز باشد، ان را با کمک تقطیر جز به جز هوای مایع تولید می نمایند. از بین ترکیبات هوا، O2 بیشترین نقطه ی جوش را دارد و در نتیجه فراریت کمتری نسبت به نیتروژن و آرگون از خود نشان میدهد
مراحل این فرایند به صورت زیر است:
گام اول: فیلتراسیون هوا و از بین بردن ناخالصی های موجود.
دوم: از بین بردن کربن دی اکسید و رطوبت با کمک جذب قلیایی
سوم: هوا فشرده می شود و حرارت حاصل از فشرده سازی با روشهای خنک سازی معمولی از بین می رود.
چهارم: هوای فشرده و خنک شده به کویل های موجود (سیم پیچ ها) ر یک محفظه منتقل می شود.
پنجم: بخشی از هوای فشرده شده (با فشار حدود 200 اتمسفر) در محفظه گسترش پیدا می کند و سیم پیچ ها را خنک می کند
ششم: گاز منبسط شده با مراحل انبساط و فشرده سازی متعاقب آن به کمپرسور برگردانده می شود که درنهایت باعث مایع شدن هوای فشرده شده در دمای 196 درجه سانتیگراد می شود
هفتم: هوای مایع حرارت داده می شود تا در ابتدا گاز های کمیاب و سبک و سپس نیتروژن تقطیر شوند و اکسیژن مایع را ترک کنند.
انجام مراحل فوق می تواند این گاز را با خلوص 99.5 درصد، و با بالاترین خلوص موجود برای اهداف صنعتی گوناگون تولید نماید
منبع : britannica.com






