
انرژی شیمیایی نوعی از انرژی است که به اتم ها و مولکول ها مربوط است. اغلب آن را به عنوان انرژی بین پیوندها و مولکول ها محدود می کنند که در واقع درست نیست و علاوه بر آن انرژی ذخیره شده در الکترون های اتم ها و یون ها نیز است.این نوع از انرژی را می توان در هنگام انجام برخی از واکنش های شیمیایی خصوصا واکنش های گرمازا مشاهده نمود.
در این واکنش ها اختلاف انرژی شکست پیوندهای قدیمی و تشکیل پیوندهای جدید خود را به شکل گرما نشان داده و آن را به محیط اطراف می دهد. شاید درک انرژی شیمیایی بر خلاف انرژی هایی مانند جنبشی و پتانسیل آسان نباشد اما این به معنا نیست که این نوع از انرژی قدرت کمی دارد ، کافی است بدانید اکثر اتومبیل ها و موتورهای جهان با این انرژی کار می کنند.
نمونه هایی از انرژی شیمیایی ذخیره شده عبارتند از نفت خام ، گاز طبیعی ، زیست توده ، باتری و زغال سنگ هستند. در بیشتر مواقع هنگامی که این نوع انرژی از یک ماده ازاد می شود به طور کامل به یک ماده جدید انتقال پیدا می کند. به عنوان مثال هنگامی که یک انفجار رخ می دهد ، انرژی شیمیایی موجود در آن به صورت گرمایی، سینتیکی و صدا به محیط اطراف منتقل می شود.
راه های آزاد شدن انرژی شیمیایی
حتما کرم های شب تاب را دیده اید که می درخشند. این حشرات در واقع انرژی شیمیایی را به نورانی تبدیل می کنند و منجر به تولید صحنه ای به این زیبایی می شوند. از طرفی بسیاری از سوخت های فسیلی که غنی از انرژی شیمیایی هستند با سوختن، انرژی خود را آزاد می کنند. البته این تنها راه آزاد کردن انرژی آن ها نیست و روش های مختلفی برای تبدیل انرژی این ترکیبات به انواع انرژی های حرکتی، الکتریکی، گرمایی و… وجود دارد. به عنوان مثال در وسایل نقلیه از انرژی ذخیره شده در سوخت های فسیلی برای حرکت این وسایل استفاده می شود و در نتیجه یک نوع تبدیل شیمیایی به حرکتی داریم.
همچنین بسیاری از این تبدیل انرژی ها در بدن ما اتفاق می افتد. به عنوان مثال انرژی ذخیره شده در پیوندهای بین مولکولی گلوکز ذخیره می شود و در نتیجه سوختن آن با اکسیژن مصرف می شود. در نتیجه زمانیکه شما می خواهید راه بروید و یا چیزی را بردارید و حمل کنید از این انرژی استفاده می کنید. در این مورد تبدیل انرژی شیمیایی به حرکتی و گرمایی اتفاق می افتد.
نمونه هایی از انرژی شیمیایی در زندگی روزانه ما
چوب :
چوب خشک هنگامی که می سوزد انرژی خود را به صورت گرما و نور به محیط می دهد. پس از سوختن نیز تبدیل به زغال می شود و باز می توان از آن برای ایجاد انرژی استفاده کرد. چرا که خود زغال نیز یک منبع انرژی محسوب می شود.
غذا :
غذایی که مصرف می کنیم یک نمونه خوب دیگر است. انرژی ذخیره شده در غذاها هنگام هضم آزاد می شود. در هنگام هضم غذاها به قطعات کوچکی تقسیم می شوند. شکسته شدن غذا به قطعات کوچکتر موجب آسان شدن فعل و انفعالات شیمیایی و ازاد شدن انرژی ذخیره شده است.
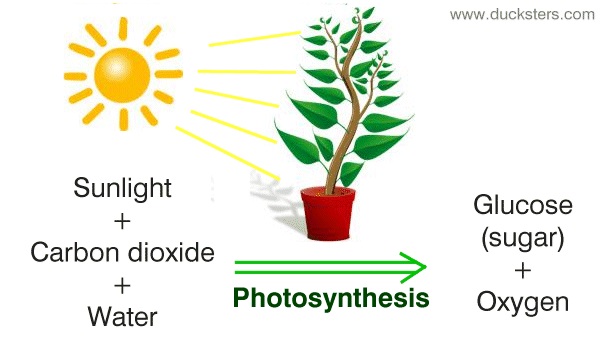
فتوسنتز :
خورشید انرژی زیادی را به زمین می رساند و عملا بدون آن زندگی بر روی زمین ممکن نیست. انرژی نورانی خورشید تاثیر بسزایی در فتوسنتز دارد، جایی که گیاه انرژی را از نور خورشید گرفته و با استفاده از آن و مواد خام ساده مانند دی اکسید کربن و آب ترکیبات پیچیده مانند گلوکز تولید می کند. همانطور که پیش از این نیز ذکر شد گلوکز انرژی شیمیایی را در پیوندهای خود ذخیره کرده و در نتیجه شکسته شدن این پیوندها انرژی مورد نیاز گیاه تامین می شود. این یک نوع تبدیل انرژی نورانی به انرژی الکتریکی است.
زغال سنگ :
زغال سنگ یک هیدروکربن است و سوزاندن آن علاوه بر تولید انرژِی نورانی و گرمایی، منجر به تولید دی اکسید کربن نیز می گردد.
نفت :
نفت یک سوخت فسیلی است ومی تواند با مصرف انرژی شیمیایی،گرما و نور ایجاد کنند. علاوه بر این می توانند به ترکیبات دیگری مانند بنزین و دیکر مشتقات نفتی تبدیل شوند.
باتری های شیمیایی :
در باتری ها، انرژی شیمیایی با روش الکترولیز به انرژی الکتریکی تبدیل شده و برق تولید می کند. اگر باتری قابل شارژ باشد، در هنگام شارژ کردن، نوع تبدیل انرژی آن الکتریکی به شیمیایی است.
زیست توده و گاز طبیعی :
از واکنش سوختن این دو ماده نیز نور و گرما آزاد می شود. در این فرآیند تبدیل انرژی شیمیایی به انرژی گرمایی و نورانی تبدیل می شود.
بیشتر بخوانید :
اسید باتری چیست و چه خطراتی دارد ؟
نحوه تبدیل انرژی شیمیایی به الکتریکی
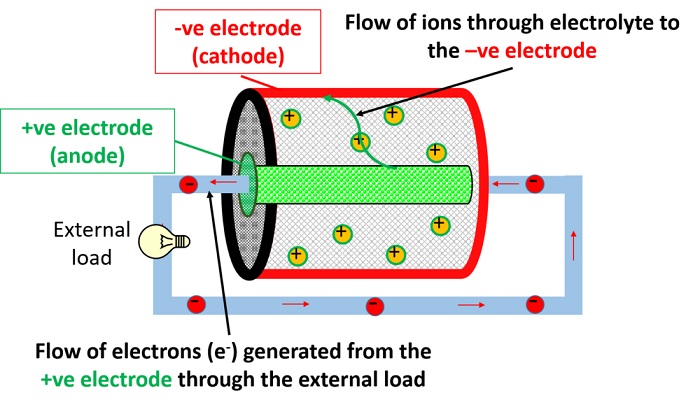
یکی از بارزترین نمودهای این تبدیل باتری ها هستند که به راحتی انرژی مکانیکی را از نوع شیمیایی تامین می کنند. انواع مختلفی از باتری ها وجود دارند که همه آنها سه جز اساسی دارند : کاتد ، آند و الکترولیت .
هنگامی که ترمینال های منفی و مثبت معمولا با یک سیم به یکدیگر وصل شوند الکترون ها (الکتریسیته) از طریق سیم بین آند و کاتد جریان پیدا می کند و واکنش های شیمیایی در الکترودها اتفاق می افتد. واکنش ها بین الکترولیت – کاتد و آند – الکترولیت اتفاق می افتند و در نتیجه الکتریسیته تولید می شود. باتری های مختلف همگی با این مکانیزم کار می کنند و تفاوت تنها در نوع آند ، کاتد و الکترولیت استفاده شده است.
باتری های یک بار مصرف تا زمانی که واکنش شیمیایی بین این سه عنصر ادامه داشته باشد کار میکنند. در باتری های قابل شارژ مجدد می توان با استفاده از الکتریسیته فرآیند را معکوس کرده و خصوصیات مواد را بازیابی کرد. باتری خودرو نمونه ای از باتری های قابل شارژ است. باتریهای دارای الکترولیت مایع را سلول مرطوب می نامند. سرب – اسید به صورت معمول در اتومبیل ها استفاده می شود که آن را سلول مرطوب می نامند. آنهایی که دارای الکترولیت جامد هستند به عنوان سلول خشک شناخته می شوند. باتری های آلکالاینی نمونه ای از سلول های خشک هستند.

سلام…ممنون خیلی خوب و آموزنده بود…