
کربنات پتاسیم به صورت پودری و مایع در گرید های خوراکی ، صنعتی و کشاورزی (کود) موجود است. جهت ثبت سفارش، فروش و خرید پتاسیم کربنات، و اطلاع از قیمت ها با مشاوران ما در موسسه مبتکران شیمی در ارتباط باشید. این محصول به دو صورت پودری (چینی) و مایع (ایتالیایی) قابل عرضه است.
فروش پتاسیم کربنات مایع و پودری :
در حال حاضر موسسه ی مبتکران شیمی به عنوان یکی از تامین کنندگان محصولات شیمیایی کشور، طیف گسترده ای از مواد شیمیایی صنعتی را از برندهای معتبر به فروش می رساند. برای کسب اطلاعات بیشتر می توانید با همکاران ما در ارتباط باشید.
خرید کربنات پتاسیم :
جهت اطلاع از نحوه ی ثبت سفارش و خرید این محصول با شماره تلفن های زیر تماس حاصل فرمایید.
| اطلاعات محصول | پودری (کربنات پتاسیم چین)
تولید کننده: چین بسته بندی: کیسه 25 کیلویی خلوص: 99.5% مایع (کربنات پتاسیم ایتالیا) تولید کننده: ساخت ایتالیا بسته بندی: بشکه 300 کیلویی خلوص: 50% CAS NO: 584-08-7 |
| آنالیز محصول | پودری (کربنات پتاسیم چین)
مایع (کربنات پتاسیم ایتالیا) |
خواص و ویژگی ها
ویژگی های این ماده را در جدول زیر می توانید مشاهده نمایید:
| فرمول شیمیایی | K2CO3 |
| جرم مولکولی | 138.205 g/mol |
| دانسیته | 2.43 g/cm³ |
| نقطه ی ذوب | 891 درجه سانتی گراد |
| شکل ظاهری | پودر یا گرانول بدون بو و سفید رنگ |
کربنات پتاسیم چیست؟
پتاسم خالص را نمی توان از کانی ها به دست اورد اما میتوان آن را از ترکیباتی مثل پتاسیم کربنات به دست آورد. منابع مهم پتاسیم و پتاس منابعی در کالیفرنیا، آلمان، نیومکزیکو، یوتا و..میباشد. در عمق 3000 فوتی زیر بستر Saskatchewan ، مقادیر عظیمی از پتاس وجود دارد که می تواند به عنوان یک منبع مهم برای این عنصر در آینده در نظر گرفته شود.
این ماده طعم نمکی دارد ، که در آب محلول است و در حلال های آلی مثل اتانول واتر و استون حل نمی شود. فشار بخار آن بسیار پایین است و نقطه ذوب آن را نمی توان تعیین کرد .محصول فوق در دمای بالا تجزیه می شود،و می تواند رطوبت هوا را جذب کند به همین دلیل ظاهری خیس و آبکی دارد و فرایند حل شدن آن در آب فرایندی گرمازا است. زمانیکه در آب حل می شود به اجزاء سازنده اش یعنی کاتیون پتاسیم (+K) و انیون کربنات (–CO32) تبدیل و محلول خاصیت قلیایی از خود نشان می دهد.
یون های K و کربنات به طور طبیعی در طبیعت وجود دارد، بنابراین این ماده با محیط زیست سازگاری دارد. وجود یون کربنات موجب افزایش pH آب می شود. بنابراین آب حاوی آن باید قبل از تخلیه به محیط زیست، تعدیل pH شود.
کربنات پتاسیم خوراکی:
این محصول در انواعی از مواد غذایی مثل تولید محصولات نانوایی استفاده می شود. همچنین پتاسیم مورد نیاز در خوراک دام ها را می توان از آن تامین کرد. گرید خوراکی آن نیز در تولید کشمش نیز استفاده می شود. برای تهیه کشمش از ترکیبی متشکل از درصد های معینی از این ماده و روغن کشمش استفاده می کنند که روش انجام این کار به قرار زیر است :
مقدار یک لیتر روغن با 2.5 کیلوگرم پتاسیم کربنات در 100 لیتر آب مخلوط می شود ، سپس انگور به مدت 30 دقیقه درون محلول قرار داده شده و سپس آن را روی رشته های سیم مفتولی آویزان می کنند تا خشک شود. با این روش کشمش سبز تولید می شود.
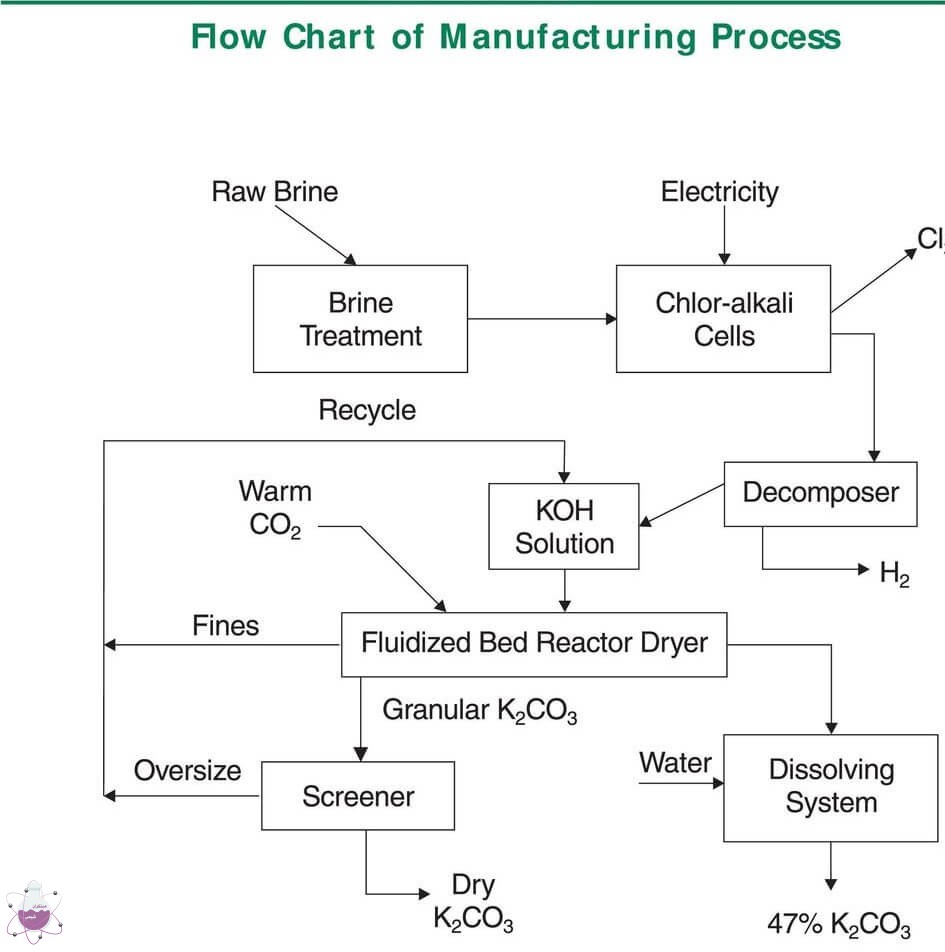
روش تولید :
این محصول فراورده و محصول تولیدی واکنش بین پتاس (KOH)مایع ،و کربن دی اکسید است .
2KOH + CO2 → K2CO3 + H2O
تولید آب در این واکنش موجب می شود که در فرآیندهای معمولی تولید ، مرحله ای هم به خارج کردن آب اختصاص داده شود . در روش جدیدی که امروزه مورد توجه قرار گرفته است ، واکنش در راکتورهای بستر سیال صورت می گیرد که در محصول نهایی آبی وجود ندارد و نیازی به عملیات خارج کردن آب وجود ندارد.
روش های جایگزین دیگری نیز مانند الکترولیز پتاسیم کلرید وجود دارد که برای تولید در مقیاس صنعتی هم می توان مورد استفاده قرار داد . زمانیکه پتاس را برای حذف ناخالصی ها در کوره حرارت می دهند ، کربنات پتاسیم نیز ساخته می شود .
کاربرد ها:
از آنجایی که این ماده کاربردهای گسترده ای دارد، گریدهای تجاری متنوعی از آن وجود دارد. مشخصه کاربردی آن، کاربرد آن در اکثر حوزه ها به ویژه شیشه، سرامیک، تولید سیلیکات پتاسیم و بی کربنات پتاسیم، مواد دارویی، صنایع غذایی ( پتاسیم کربنات خوراکی )، شوینده ها و پاک کننده ها، مواد شیمیایی عکس برداری، کودها و آفت کش های کشاورزی، خالص سازی گاز، افزودنی های لاستیک، کریستال های پلیمری، بازدارنده های خوردگی، سیمان و منسوجات را ممکن می سازد. در مورد گرید خوراکی این ماده پیش تر صحبت شد و در ادامه به سایر موارد خواهیم پرداخت .
فروش کربنات پتاسیم با بهترین قیمت در مبتکران شیمی
صنایع غذایی :
به طور کلی ترکیبات حاوی پتاسیم برای بدن انسان مفید هستند و باعث افزایش تراکم استخوان، سلامتی قلب و عروق و… می شوند، پتاسیم کربنات نیز به عنوان عامل تنظیم اسیدیته مواد غذایی و در تولید نوشابه، شکلات ، شیرینی پزی ، تهیه پودر کاستارد و…به عنوان افزودنی استفاده می شود.همچنین از این ماده شیمیایی در تهیه مکمل های ورزشی نیز استفاده می شود.

آیا استفاده از کربنات پتاسیم به عنوان افزودنی مفید است؟
این ترکیب شیمیایی به عنوان یک افزودنی ایمن در سازمانهای غذا و دارو در اروپا و آمریکا شناخته می شود و در اثر استفاده از آن به عنوان افزودنی صنایع غذایی هیچ تاثیر نامطلوب و مخربی گزارش نشده است ، بر اساس توصیه FDA میزان مصرف مجاز این ماده به مقدار 100 میلی گرم در هر دوز می باشد و مصرف آن در دوز های بالا در مکمل های ورزشی می تواند باعث ایجاد اسهال ، شکم درد، استفراغ و حالت تهوع شود . استفاده از مواد غذایی حاوی این ماده نیز برای زنان در دوره بارداری و شیردهی توصیه نمی شود.
شیشه سازی
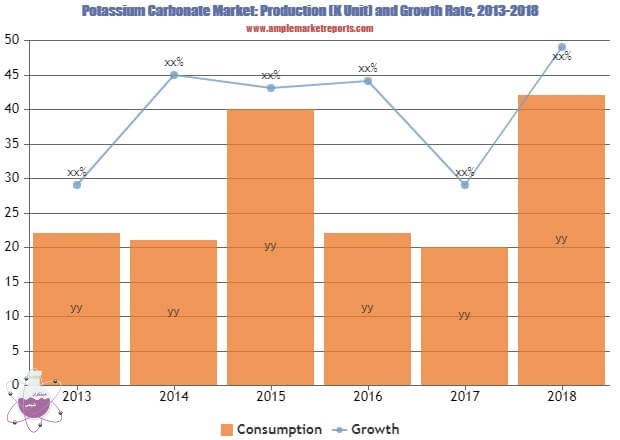
بیشترین کاربرد پتاسیم کربنات در صنعت شیشه سازی است به گونه ای که بیش از 40 درصد تقاضا و مصرف را به خود اختصاص داده است. صنعت سرامیک نیز دومین مصرف کننده این ماده با سهم 10 درصدی است. دلیل اصلی اینکه از چنین ماده گرانی به جای سودا اش در صنعت شیشه سازی استفاده می شود ، سازگاری بیشتر با اکسیدهای سرب، باریم و استرانسیوم است.
از ویژگی های شیشه های تولید شده با این روش می توان به مقاومت الکتریکی بیشتر، ضریب انکسار بالاتر، درخشندگی بیشتر و کارایی در محدوده دمایی بالاتر اشاره نمود. علاوه بر این باعث بهبود رفتار رنگ ها در شیشه می شود.
کربنات پتاسیم در کشاورزی
یکی از کاربردهای مهم این ماده توانایی آن برای تولید کود است. محصول فوق به دلیل داشتن یون K به رشد گیاهان و حفظ آب در خاک کمک می کند و باعث تقویت ریشه و ساقه ی گیاهان می شود.
برخی کشاورزان با مشکل پایین بودن pH خاک مواجه می باشند. گاهی خاک ها به طور طبیعی اسیدی هستند علاوه بر این کود دهی و آبیاری به طور طولانی مدت نیز می تواند موجب کاهش pH و اسیدی شدن خاک نیز گردد. pH خاک زیر 5.5 ممکن است منجر به کاهش بازده و خسارت به محصول شود. در این شرایط گیاه برای جذب ریز مغذی هایی مانند منگنز ، آلومینیوم و آهن با مشکل مواجه خواهد شد و همچنین ممکن است مشکل مسمومیت مبکروارگانیسم ها نیز رخ دهد و گیاه در جذب مواد مغذی مهمی مانند منیزیم، کلسیم و پتاسیم با مشکل مواجه شود و آسیب های جدی ای ببیند.
-
اما راهکار چیست؟
برای این منظور خاک را با کمک سایر مواد شیمیایی قلیایی تر می نمایند تا گیاه راحت تر رشد نماید و مواد مغذی به راحتی در اختیار آن قرار بگیرد. آهک یکی از موادی است که برای این منظور به وفور مورد استفاده قرار می گیرد. اما این ماده انحلال پذیری کمی دارد. بر خلاف آهک ، کربنات پتاسیم بسیار محلول است و بنابراین در آبیاری قطره ای نیز قابل استفاده است.
به دلیل حلالیت زیاد ، این ماده می تواند به همراه آب به تمام نقاط ریشه منتقل شود و به مناطق عمیقتر خاک برود. این ماده به سرعت در واکنش های شیمیایی در اطراف ریشه تأثیر می گذارد و pH آن ناحیه را بالا می برد.
استفاده از محصول فوق به صورت دوره ای ، یا حتی به طور منظم ، به عنوان بخشی از برنامه رشد گیاه ، می تواند از افت pH جلوگیری کند.
ترکیبات صنعتی :
برای تولید ترکیبات شیمیایی متفاوت از این ماده استفاده می شود. صابونی که در تهیه آن از این ماده استفاده شده نسبت به صابون به دست امده از سدیم کربنات ملایم تر است.
کاربرد اصلی کربنات پتاسیم برای تولید شیشه به خصوص لنز نوری ،صفحه تلوزیون ،و لوله پرتو کاتدی است .جدای از این ها،از این ماده در ساخت جوهر چاپ و پیگمنت ها نیز استفاده می شود. در صنعت سفالگری آن را به عنوان یک ماده شیمیایی برای لعاب گلدان استفاده می کنند
کاربردهای دیگر آن ، ،در صنعت عکاسی و تولید نمک پتاسیم و…است.
هرگاه از عوامل خشک کننده ای مثل کلسیم کلرید و سولفات منیزیم در محلول به هر دلیلی نمی توان استفاده کرد، پتاسیم کربنات را به عنوان خشک کننده ملایم می توان به کار برد . این ماده برای ترکیبات اسیدی مناسب نیست اما برای خشک کردن فاز الی اگر مقدار بسیار کمی ناخالصی اسیدی داشته باشد استفاده می شود. همچنین برای خشک کردن بعضی از کتون ها،الکل ها،و آمین ها قبل ازتقطیر استفاده می شود.
-
رفع سختی آب
از این ماده برای رفع سختی آب نیز استفاده می شود به طوریکه از تجمع یون های Ca و Mg که دو عامل اصلی سختی آب هستند جلوگیری می کند.این ماده در غلظت بالا موجب تحریک پوست می شود، اما در غلظت های کم و متوسط برای سلامتی انسان ضرری ندارد. این محصول در محیط زیست تجزیه می شود و بنابراین چندان مقاوم نیست و در اندام ها تجمع نمی کند.
ماده ی فوق در خاموش کردن شعله های آتش با حرارت بالا استفاده می شود . این ماده برای خاموش کردن آتش و جلوگیری از گسترش آتش بسیار مفید می باشد. تاثیر این ماده در فرونشانی آتشهای نفتی و گازی نسبت به سدیم بی کربنات بیشتر است.
msds و ایمنی استفاده از کربنات پتاسیم:
این ماده در غلظت بالا موجب تحریک می شود، اما در غلظت های کم و متوسط برای سلامتی انسان ضرری ندارد.
اثرات جانبی
- در صورت برخورد با پوست باعث تحریک شده و می تواند باعث آسیب شدید چشم شود .
- اشتنشاق غبار و اسپری این ماده می تواند باعث ایجاد مشکلات شدید در سیستم تنفسی شود ( میزان آسیب بستگی به شدت تماس دارد).
- بلع کربنات پتاسیم می تواند باعث تخریب غشای مخازی دهان ، گلو ، مری و معده شود .
- هنوز در مورد این ماده گزارشاتی مبنی بر اثرات مزمن و یا ایجاد سرطان ارائه نشده است.
اثرات محیط زیستی
پتاسیم کربنات سمیت پایینی برای محیط زیست دارد. یون های پتاسیم و کربنات به وفور در محیط وجود دارند و ورود آن به محیط زیست اثر ناچیزی دارد. یون های کربنات می توانند باعث بالا رفتن pH آب شوند اما این افزایش ناچیز است. با این حال باید pH پساب اندازه گیری شود تا از بالا نبودن آن اطمینان حاصل شود.
تماس با سایر مواد شیمیایی
در تماس با اسیدها و آتش گاز کربن دی اکسید آزاد می شود. تجزیه حرارتی می تواند منجر به تشکیل اکسید پتاسیم نیز شود. کربنات پتاسیم با اسیدها، منیزیم، آلومینیوم ، مس، سرب، قلع، روی و یا سایر آلیاژها و فلزات حساس به محیط های قلیایی ناسازگاری دارد و باید از تماس آنها خودداری نمود.
برای مشاهده msds این ماده اینجا کلیک کنید .



