
سوخت آمونیوم نیترات (ammonium nitrate) که با نام آنفو نیز شناخته می شود , یک نمک آمونیومی از نیتریک اسید است. این ماده ممکن است بهصورت مایع، حاوی ذرات جامد یا پودر کریستالی سفید یا بیرنگ و بدون بو در دسترس باشد. انحلال آمونیوم نیترات در آب گرماگیر می باشد.
این محصول در حال حاضر موجود نیست.
لطفا تماس حاصل نفرمایید. با تشکر
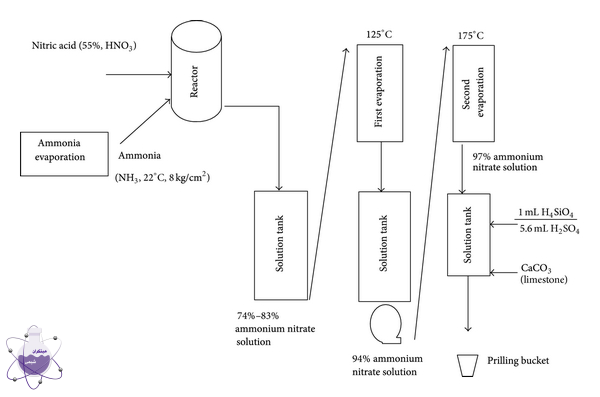
تولید نیترات آمونیوم :
این ماده با خنثی کردن اسید نیتریک (HNO3) با آمونیاک (NH3) به دست میآید. تمامی واحدهای تولید این محصول محلول نیترات آمونیوم آبی را از طریق واکنش آمونیاک که یک ماده قلیایی و اسید نیتریک در یک فرایند خنثی شدن و تشکیل نمک تولید میکنند.
واکنش تشکیل آمونیوم نیترات :
Ammonia + nitric acid → ammonium nitrate
(NH3 (aq) + HNO3 (aq) → NH4NO3 (aq
کاربرد آمونیوم نیترات :
پیش از جنگ جهانی دوم از این ماده استفادههای بسیاری از کاربرد انفجاری این ماده میشد که در قسمتهای بعدی به آن خواهیم پرداخت، اما با پایان یافتن جنگ تولید کود شیمیایی از این ماده بسیار فراگیر شد و بسیار مورداستفاده قرار گرفت.
کود معدنی این محصول وقتی شکل میگیرد که قطرات تغلیظ شده محلول آمونیوم نیترات 95 تا 99 درصد از بالای برج به سمت پایین به حرکت درمیآیند و خشک میشوند.
به علت هیدروسکوپیک (hygroscopic) بودن و جاذب رطوبت بودن این ماده معمولاً برای نگهداری و بستهبندی آن کیسههای مهرومومشده استفاده میشود. همچنین برای نچسبیدن دانههای کود به هم از یک واسطه ضد چسبندگی هم استفاده میگردد. برای کاهش و یا از بین بردن خاصیت انفجاری و مناسب شدن برای کاربری کود شیمیایی قبل از جامد شدن مقدار کمی کربنات معدنی به محلول اضافه میشود تا غلظت نیتروژن خیلی کم شود.
کود نیترات آمونیوم مایع :
این شکل از کود بهطورکلی در ترکیب با اوره فروخته میشود و به آن بهاختصار UAN گفته میشود. در بسیاری از مناطق به دلیل مشکلات حملونقل و بستهبندی شکل جامد آن متداول شده است.
در این قسمت درباره خاصیت انفجاری آمونیوم نیترات مطالبی را خواهیم خواند:
واکنش حل شدن نیترات آمونیوم در آب :
وقتی این ماده در آب حل میشود به علت گرماگیر بود واکنش در اطراف آن احساس سرما میکنید. واکنش انحلال آمونیوم نیترات را در زیر مشاهده میکنید.
(NH4NO3 (s) → NH4+ (aq) + NO3– (aq
اگر بهآرامی نیترات آمونیوم را که در آب حلشده است حرارت داده شود، محلول شروع به تجزیه شدن میکند تا وقتیکه اکسید نیتروژن آزاد شود. معمولاً این گاز خاصیت خندهآور بودن دارد. این تجزیهوتحلیل بهعنوان تجزیه حرارتی شناخته میشود و این روند نیاز به دمای بین 180 درجه سانتیگراد (356 درجه فارنهایت) تا 250 درجه سانتیگراد (482 درجه فارنهایت) دارد.
این واکنش فقط باید تحت شرایط کنترلشده و با نظارت در یک آزمایشگاه شیمی انجام شود، زیرا نیترات آمونیوم میتواند باعث آسیبدیدگی شود و درصورتیکه بیشازحد از آن استفاده شود و یا در دمای بالا قرار بگیرد باعث انفجار میشود.
آنفو یا سوخت آمونیوم نیترات :
به علت پایین بودن خاصیت انفجاری این محصول به آن روغنهای معدنی (از هیدروکربنهای سنگین تشکیلشدهاند) اضافه میکنند. روغن سوخت آمونیوم نیترات که بهاختصار ANFO مینامند مخلوطی از نیترات آمونیوم و روغن معدنی است. دسترسی آسان به این ماده باعث میشود تا آن را بهطور کنترلشده در معدنهای روباز و ساخت تونل مورداستفاده قرار گیرد. واکنش اولیه در زمان انفجار، تجزیه هیدروکربن و نیترات آمونیوم به دیاکسید کربن (CO2)، نیتروژن و آب است.
بازار آمونیوم نیترات در سطح جهانی:
کود نیترات آمونیوم همیشه محبوب بوده است اما به علت انفجارهای صورت گرفته در بعضی مناطق جهان دولتها قوانین حملونقلی سختگیرانِ تری نسبت به این محصول داشته داند و همین از محبوبیت این ماده کاسته است.
مصرف AN و سایر کودهای نیتروژن دار در کشورهای اروپای غربی و سایر مناطق به دلیل تغییرات در سیاستهای یارانه کشاورزی کاهشیافته است.
کود اوره به جایگزین محبوب کود نیتروژن تبدیلشده است، زیرا مسائل ایمنی سختگیرانهای وجود ندارد، محتوای نیتروژن بالاتری دارد و معمولاً ارزانتر است.
ازلحاظ تاریخی، کشورهای اروپای شرقی و غربی (اتحاد جماهیر شوروی سابق) از مناطق اصلی مصرفکننده بودهاند، اما نرخ مصرف در ایالاتمتحده، اروپای مرکزی، کشور چین، آمریکای مرکزی و جنوبی و آفریقا روند افزایشی داشته است. در سال 2015، این کشورها باهم بیش از 82 درصد کل مصرف جهان را تشکیل میدادند.
تخمین زده میشود میزان مصرف در سال 2015 تا سال 2020 به میزان 2.3 درصد افزایش یابد. پیشبینی میشود کشورهای چین، جنوب غربی آسیا و آسیای جنوب شرقی که بیشترین تغییر مصرف را داشته باشند.
لازم به ذکر است مصرف نیترات آمونیوم در مناطق مختلف متفاوت است، اما میانگین مصرف جهانی در کاربردیهای این ماده شامل کود از 65 درصد برای تولید کود و در کاربردهای صنعتی و انفجاری 35 درصد برای کاربردهای صنعتی و انفجاری (98 درصد) است.
درنتیجه تا سال 2020 به علت پیشرفت استفاده از کود اوره روند افزایشی این کود تنها 2 درصد خواهد بود.
ایمنی:
به علت اکسیدکنندگی بالای این ماده قابلیت انفجاری بالای دارد. همچنین تماس آن با چشم باعث آسیب جدی میشود. لطفاً پیش از تماس با این محصول نکات ایمنی آن را با دقت مطالعه فرمایید.
منابع:
Ammonium nitrate. (n.d.). Retrieved January 1, 2019, from https://pubchem.ncbi.nlm.nih.gov/compound/ammonium_nitrate#section=GHS-Classification
(n.d.). Retrieved January 1, 2019, from https://www.cropnutrition.com/ammonium-nit
Hazardous Substances Data Bank (HSDB). (n.d.). Retrieved January 1, 2019, from https://toxnet.nlm.nih.gov/cgi-bin/sis/search2/r?dbs hsdb:@term @rn @rel 6484-52-2
Ammonium Nitrate. (n.d.). Retrieved January 1, 2019, from https://ihsmarkit.com/products/ammonium-nitrate-chemical-economics-handbook.html


با سلام قیمت نیترات امونیوم ۹۵درصد در بازار جهانی لطف کنید قیمت اگه دارید به ایمیل بنده بفرستیدتشکر
سلام، لطفا برای اطلاع از قیمت و استعلام موجودی با شماره های موجود در بخش تماس با ما سایت، تماس حاصل فرمایید.
سلام لطفا قیمت امونیوم نیترات
با سلام. لطفا جهت اطلاع از قیمت ها با دفاتر فروش ما تماس حاصل فرمایید.
سلام لطفا قیمت امونیوم نیترات را اعلام کنید .